Замедление - реакция
Cтраница 2
Четырехкратное замедление реакции при введении дейтерия свидетельствует о том, что протон отрывается в стадии, определяющей скорость реакции. В этих случаях, по-видимому, происходит отрыв атома водорода с образованием свободного радикала, который подвергается дальнейшему окислению неорганическими частицами. [16]
Замедление реакции гидролиза с увеличением степени полимеризации вызвано происходящим при этом затруднением нуклеофиль-ной атаки атомов кремния. [17]
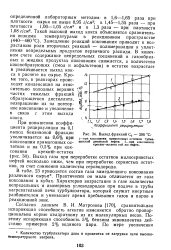 |
Выход фракций С5 - 200 С. [18] |
Замедление реакций коксования приводит к возрастанию роли вторичных реакций - полимеризации и уплотнения непредельных продуктов первичного распада. В конечном счете содержание непредельных соединений в газообразных и жидких продуктах коксования снижается, а количество коксообразующих ( смол и асфальтенов) в остатке возрастает и увеличивается выход кокса в расчете на сырье. [19]
Замедление реакции гидролиза с увеличением степени полимеризации объясняется происходящим при этом затруднением нуклеофильной атаки атомов кремния. [20]
Замедление реакций распада алканов вдали от равновесных состояний объясняется тем, что крекинг протекает по цепному механизму и замедляется в результате обрыва цепей в объеме на молекулах тормозящих продуктов. Подтверждением этого представления явились опыты по влиянию продуктов распада [48] и обнаружение ингибиторов реакций крекинга - пропилен, изобутилен, аллен, триметил-этилен, N0 и др. [48-50, 54-58, 153], что дало несомненное доказательство цепной природы этих реакций. [21]
 |
Влияние состава растворителя на константу. [22] |
Замедлению реакции, что качественно соответствует электростатической концепции. В промежуточной области концентраций при значении мольной доли ацетона 0 2 - 0 5 преобладающее влияние-оказывает накапливание воды и очень хорошо растворимого в ней ацетамида в твердой фазе, что приводит к росту скорости гидролиза, несмотря на снижение диэлектрической проницаемости жидкой фазы. [23]
После замедления реакции прекращают охлаждение смеси и дают ей нагреться. Выделяющийся газ конденсируют после предварительной промывки водой. Конденсацию проводят в трех ловушках, охлаждаемых до температуры от - 25 до - 30 С. [24]
Для замедления реакции карбонил никеля разбавляют четьь-реххлористым углеродом или хлороформом. [25]
Для замедления реакции и более равномерного распределения MgO в реакционной смеси препарат иногда вводят в реактор в виде 50 % - ной водной суспензии. Для получения магнийфосфатных связующих с мольным отношением PgOs / MgO, равным 5 5, растворение MgO в Н3РО4 проводят при 20 - 25 С. При концентрировании исходных растворов нагреванием при 80 С образуются более устойчивые пересыщенные ме-тастабильные растворы. [26]
Такое замедление реакции затем может сопровождаться внезапным взрывом. Во избежание этого используют следующий прием: к тонкоизмельчеино-му LiH прибавляют сначала 200 мл эфира, а затем раствор 3 г LiAlH4 в 30 мл эфира, который инициирует начало реакции. [27]
Для замедления реакции кислот с породой и закачки активного раствора в удаленную зону пласта в него необходимо добавлять 5 % уксусной кислоты. [28]
После замедления реакции стенки стакана смывают водой и нагревают до полного разложения пробы. Раствор переводят в делительную воронку емкостью 200 - 300 мл, прибавляют 3 мл раствора диметилглиоксима, 4 мл хлороформа и сильно встряхивают в течение 1 - 2 мин. [29]
Для замедления реакции полного окисления к исходному сырью добавляют такие ингибиторы, как тетраэтилсвинец, дибромэтан, бензол, этанол, хлордифенил, хлорполифенил, этиленхлоргидрин, а при работе в кипящем слое используют твердые галогенпроизводные. [30]
Страницы: 1 2 3 4