Потенциал - осаждение - металл
Cтраница 1
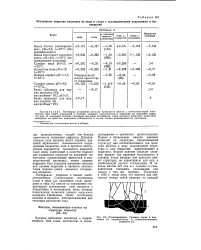 |
Псевдоморфизм. Границы зерен в подложке ( / продолжаются в электролитическое покрытие ( 2. [1] |
Потенциал осаждения металла приводится вместе с соответствующей плотностью тока ( А / м2), указанной в скобках; толщина гальванического покрытия на подложке равна 2 5 мкм. В последней колонке приведено значение потенциала, ниже которого возможно выделение водорода; на практике выделение наблюдается в случае только медноцианистых растворов. [2]
Потенциал осаждения металла из комплекса отличается от потенциала выделения металла из простых солей. Координация аддендов ионами металлов-комплексообразователей приводит к изменению величины потенциала выделения металла. Причем потенциал выделения из однотипных комплексов для разных металлов сдвигается в различной степени в зависимости от прочности образующихся комплексов. Поэтому становится возможным электролитическое разделение этих металлов электролизом растворов их координационных соединений. С другой стороны потенциалы осаждения металлов в результате образования комплексов могут быть сближены. Электролиз растворов таких комплексов приводит к выделению сплавов. Например, в присутствии избытка цианид-иона удается электролитически отделить железо от цинка, тогда как при электролизе циаяидсодер-жащих растворов меди и цинка выделяется латунь. [3]
Потенциал осаждения металла фл в ходе электролиза остается более положительным, чем потенциал выделения водорода при всех значениях применяемых плотностей тока ( фиг. Этот случай имеет место при электроосаждении серебра, золота, меди, свинца и некоторых других электроположительных металлов, потенциалы выделения которых значительно отличаются от потенциала выделения водорода. [4]
Потенциал разряжения катиона иногда называют потенциалом осаждения металла. Это тот минимальный потенциал, который должен быть приложен к электроду для того, чтобы катион потерял заряд и произошло осаждение металла. Для некоторых ионов ( Fe2, Cu2, Ag, Cd2) потенциал осаждения близок к электродному потенциалу, для других же ионов ( Fe2, Со2, № 2) потенциалы осаждения значительно превышают электродные потенциалы металлов - для электролиза необходимо определенное перенапряжение. [5]
Если при данных условиях потенциалы осаждения двух металлов близки между собой, то можно изменить эти условия таким образом, что разность потенциалов осаждения металлов станет достаточной для разделения. [6]
Субпотенциальное осаждение атомов металла: за счет энергии взаимодействия разрядившихся адсорбированных атомов металла с чужеродной подложкой катодный процесс разряда ограниченного количества ионов металла с образованием адато-мов возможен при потенциалах, более положительных, чем равновесный потенциал данной системы и потенциал стационарного осаждения металла. [7]
Изучена зависимость между интенсивностью перемешивания электролита в прикатодном слое и скоростью реакций восстановления хромовой кислоты. Показано, что в области потенциалов осаждения металла перемешивание не оказывает влияние на реакции, протекающие совместно. [8]
Совместное осаждение металлов в данном случае облегчается по мере повышения плотности тока, с увеличением которой возрастает и содержание более электроотрицательного металла в сплаве. Следует, однако, иметь в виду, что применение высоких плотностей тока, приближающихся к значению предельного тока или превышающих его, может неблагоприятно сказаться на качестве покрытия, особенно если осаждение сплава производится на сильно профилированных изделиях. Можно использовать другой путь, а именно: сблизить потенциалы осаждения металлов Mt и М2, соответствующим образом изменяя концентрацию ( активность) ионов этих металлов в электролите. [9]
Совместное осаждение металлов в данном случае облегчается по мере повышения плотности тока, с увеличением которой возрастает и содержание более электроотрицательного металла в сплаве. Следует, однако, иметь в виду, что применение высоких плотностей тока, приближающихся к значению предельного тока или превышающих его, может неблагоприятно сказаться на качестве покрытия, особенно, если осаждение сплава производится на сильно профилированных изделиях. Можно использовать другой путь, а именно: сблизить потенциалы осаждения металлов Мг и М2, соответствующим образом изменяя концентрацию ( активность) ионов этих металлов в электролите. [10]
Следует отметить, что кроющая способность отличается от рассеивающей способности. Первая дает представление о том, в какой степени электролит способен покрыть всю поверхность изделия независимо от толщины покрытия, вторая - о количественном распределении металлического покрытия на поверхности изделий. Поэтому на величину кроющей способности влияют многие другие факторы, обычно не сказывающиеся на рассеивающей способности электролита. К ним следует отнести прежде всего природу металла изделия, качество его обработки и другие факторы, влияющие на перенапряжение водорода и потенциал осаждения металла. [11]
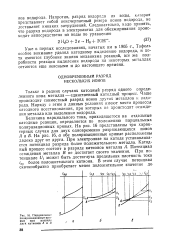 |
Парциальные поляризационные кривые при разряде двух катионов А я В. [12] |
Величина парциального тока, приходящегося на отдельные катодные реакции, определяется по положению парциальных поляризационных кривых. На рис. 16, а обе поляризационные кривые расположены далеко друг от друга. При электролизе на катоде устанавливается потенциал разряда более положительного металла. Катодный процесс состоит в разряде катионов металла А. Потенциал осаждения металла В не достигает своего значения. При потенциале L / i может быть достигнута предельная плотность тока ( пр более положительного катиона. [13]
Потенциал осаждения металла из комплекса отличается от потенциала выделения металла из простых солей. Координация аддендов ионами металлов-комплексообразователей приводит к изменению величины потенциала выделения металла. Причем потенциал выделения из однотипных комплексов для разных металлов сдвигается в различной степени в зависимости от прочности образующихся комплексов. Поэтому становится возможным электролитическое разделение этих металлов электролизом растворов их координационных соединений. С другой стороны потенциалы осаждения металлов в результате образования комплексов могут быть сближены. Электролиз растворов таких комплексов приводит к выделению сплавов. Например, в присутствии избытка цианид-иона удается электролитически отделить железо от цинка, тогда как при электролизе циаяидсодер-жащих растворов меди и цинка выделяется латунь. [14]
Страницы: 1