Потенциал - отталкивание
Cтраница 2
В результате возникает потенциал отталкивания, зависимость которого от межатомного расстояния должна быть такой, чтобы он превалировал на малых расстояниях и был меньше потенциала притяжения на больших расстояниях. Обычно его записывают либо как 5 / R12, либо Яехр ( - / р), где В, К и р - некоторые константы. [16]
В этой работе потенциал отталкивания несвязанных атомов и групп находился из второго вириального коэффициента для реального газа, состоящего из атомов или молекул, имеющих электронное строение, сходное со строением рассматриваемых атомов и групп. [17]
 |
Схематичное представление энергии межмолекулярного взаимодействия. [18] |
Точное выражение для потенциала отталкивания неизвестно. Часто для удобства энергию отталкивания считают обратно пропорциональной двенадцатой степени межмолекулярного расстояния. [19]
Такое выражение для потенциала отталкивания имеет известные теоретические преимущества. [20]
В качестве примера рассмотрим потенциал отталкивания Не - - - Не, определенный различными методами. [21]
Предложен способ описания зависимости потенциала отталкивания от колебательных координат, основанный на использовании dumbbell модели. Проведен расчет смещения основной колебательной полосы молекулы водорода при растворении в сжиженных благородных газах с учетом различного относительного изменения сил отталкивания н притяжения при оптическом возбуждении молекул. [22]
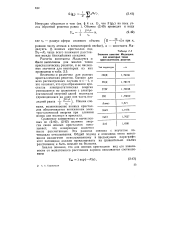 |
Значение констант Маделунга. [23] |
Эта разница связана с неучетом потенциала отталкивания. Общий подход к описанию этого потенциала аналогичен использованному в предыдущем параграфе: этот потенциал должен превалировать на сравнительно малых расстояниях и быть меньше на больших. [24]
Если молекулы не являются сферическими, потенциал отталкивания зависит не только от расстояния, но и от взаимной ориентации молекул. Симметрия отталкивательных сил должна соответствовать симметрии ядерных остовов. [25]
Если молекулы не являются сферическими, потенциал отталкивания зависит не только от расстояния, но и от взаимной ориентации молекул. Симметрия отталкивательных сил должна соответствовать симметрии ядерных остовов. В модельных потенциалах асимметрия отталкивательных сил часто передается тем, что молекулам приписывают форму твердых стержней, эллипсоидов и др. Взаимодействие между двух - и многоатомными молекулами может быть описано и с так называемых атом-атом потенциалов, о которых несколько робнее см. в § 4 настоящей главы. [26]
На практике обнаружены примеры действия как потенциала отталкивания, так и потенциала притяжения и в некоторых случаях их влияние прослежено для различных матриц. Это может быть связано с разной длиной связи молекулы в двух состояниях. [27]
Если частицы взаимодействуют друг с другом посредством короткодействующего потенциала отталкивания, то связанные с взаимодействием эффекты могут быть выражены через ампли - ТУДУ а - рассеяния двух частиц друг на друге. [28]
Для большинства ионных кристаллов показатель я в потенциале отталкивания велик ( см. задачу 3.2), так что в первом приближении можно рассматривать положительные и отрицательные ионы в таких кристаллах, как жесткие шары с радиусами / и г соответственно. [29]
Для большинства ионных кристаллов показатель п в потенциале отталкивания велик ( см. задачу 3.2), так что в первом приближении можно рассматривать положительные и отрицательные ионы в таких кристаллах, как жесткие шары с радиусами г и / соответственно. [30]
Страницы: 1 2 3 4