Потенциал - появление - молекулярный ион
Cтраница 1
Потенциал появления молекулярных ионов, определенный методом электронного удара, совпадает с адиабатическим в том случае, если равновесные межъядерные расстояния в молекуле и молекулярном ионе равны. [1]
Потенциалы появления молекулярного иона и осколочных ионов при ионизации в электронном пучке приведены в табл. 11.96. Там же даны потенциалы ионизации соответствующих радикалов. [2]
 |
Схема образования колебательно-возбужденного молекулярного иона при. [3] |
Следовательно, потенциалы появления молекулярных ионов не совпадают с потенциалами ионизации молекул, а почти всегда несколько больше последних. [4]
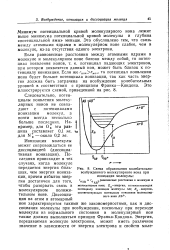 |
Схема образования колебательно-возбужденного молекулярного иона при ионизации молекулы. [5] |
Следовательно, потенциалы появления молекулярных ионов не совпадают с потенциалами ионизации молекул, а почти всегда несколько больше последних. [6]
Потенциал появления каждого осколка должен быть равен потенциалу появления молекулярного иона плюс е0, соответствующее переходному состоянию; потенциал появления может быть больше термодинамической величины, если существует энергия активации для реакции рекомбинации. На практике точный расчет Q и Q не может быть сделан, но Розенсток и сотрудники упростили задачу, приняв, что колебания ядер должны быть одинаковыми во всех допустимых электронных состояниях молекулярного иона и что любая энергия выше минимума на потенциальной поверхности переходит в движение ядра. [7]
Реакция образования аммиака в азото-водородной смеси начинается при потенциале появления молекулярных ионов азота. Ускорение реакции наблюдается при образовании атомарных ионов и атомов азота. [8]
Увеличение чувствительности, достигнутое благодаря длинным щелям, сделало возможным измерение потенциала появления молекулярного иона водорода - измерение, которое требует высокой чувствительности, но очень низкого разрешения. [9]
На этом основании потенциал появления осколочных ионов, так же как и потенциал появления молекулярных ионов, определяемых этим методом, может рассматриваться, как верхний предел адиабатической или истинной величины. На рис. 178 и 179 представлены ионизационные кривые для ртути с анализом по массам образующихся продуктов, а также без него. На кривой для Hg наблюдается максимум, соответствующий примерно 50 эв, и последующее постепенное падение интенсивности ионного тока примерно на 40 % от максимальной величины при 400 эв. Кривые для соответствующих многозарядных ионов характеризуются максимумами при постепенно повышающихся значениях энергии электронов. Форма кривой на рис. 179 типична для больших молекул органических соединений. В этих случаях преимущественно образуются не молекулярные, а осколочные ионы. Доля многозарядных ионов меньше, чем для одноатомных газов, что отражает возрастающую вероятность диссоциации при высоких энергиях электронов. Наибольшая эффективность ионизации обычно наблюдается в области 50 - 100 эв [1987]; на этом основании энергии такого порядка используются при химическом анализе. [10]
Кэрисс и Райдил [21] я Бритт [4], применяя медленные электроны, установили, что реакция образования аммиака в азото-аодородной смеси начинается при потенциале появления молекулярных ионов азота. [11]
Кэрисс и Райдил [21] и Бритт [4], применяя медленные электроны, установили, что реакция образования а-ммиака в азото-водородной смеси начинается при потенциале появления молекулярных ионов азота. [12]
 |
Ионы, образующиеся при раДиолизе воДы, и их потенциалы появления. [13] |
В общем случае чем меньше потенциал появления иона, тем в большем количестве он образуется. Это правило не выполняется для О, если только не принять, что значительная часть ионов О образуется по второму приведенному в таблице процессу. Для самой воды потенциал появления молекулярного иона ( 13 эв) и ионизационный потенциал ( 12 56 эв) практически одинаковы, что связано с отсутствием других потребляющих энергию процессов. Это, однако, не относится ко всем другим ионам, где ионизационный потенциал на 5 - 8 эв ниже потенциала появления. [14]
Предлагались различные методы анализа смесей, компоненты которых отличаются только по изотопному составу. Теоретически возможно, применяя высокое разрешение, разделить многие пики в масс-спектрах таких смесей. Разность масс Н2 и D составляет только 1 55 - 10 - 3 а. Разность масс СН - 13С составляет 4 48 - Ю-3 а. Несмотря на то, что потенциалы появления молекулярных ионов близки, потенциал появления иона ( CH2D) из монодейтерометана почти на 1 эв больше, чем для метана [1944]; это обеспечивает возможность определения молекулярных ионов при использовании низких энергий ионизирующих электронов без помех, обусловленных осколками других присутствующих соединений. [15]
Страницы: 1