Анодный замедлитель
Cтраница 2
Попытки комбинирования этих замедлителей привели к неожиданному открытию, что совместное применение двух таких анодных замедлителей, как хромат и фосфат, при соответствующей величине рН среды обеспечивает резкое ослабление или полное устранение ( при значительно меньшем расходе реагентов) всех отрицательных явлений, указанных выше. Ведутся исследования в области подыскания новых комбинаций различных замедлителей коррозии. [16]
Таким образом, хроматы являются одним из наиболее активных замедлителей коррозии; однако, как и при всех анодных замедлителях, при концентрации хроматоа недостаточной для полного прекращения общей коррозии, возникают язвенная коррозия и наросты ржавчины, вызывающие образование-свищей и увеличение потерь напора в трубопроводах. [17]
 |
Зависимость коррозионного растрескивания от содержания никеля в стали, содержащей 18 % Сги 0 05 % С. [18] |
В том случае, когда основная часть поверхности металла может сохранять пассивное состояние, в щелях и зазорах вследствие затруднения диффузии окислителя и анодного замедлителя возникает активное состояние. Установлено, что уменьшение концентрации пассивирующих агентов в щели приводит к постепенной потере металлом пассивного состояния и к сильному разблаго-роживанию потенциала. Это явление может быть также объяснено с помощью дифференциальных анодных и катодных кривых. [19]
В том случае, когда основная часть поверхности металла может сохранять пассивное состояние, в щелях и зазорах вследствие затруднения диффузии окислителя и анодного замедлителя возникает активное состояние. Установлено, что уменьшение концентрации пассивирующих агентов в щели приводит к постепенной потере метал - лом пассивного состояния и к сильному разблагороживанию потенциала. Это явление может быть также объяснено с помощью дифференциальных анодных и катодных кривых. [20]
Одним из эффективных методов борьбы с экстрагивной коррозией является перевод всех атомов твердого раствора в пассивное состояние, повышение перенапряжения анодного процесса активных атомов путем введения анодных замедлителей, применение электрохимической защиты, изоляция от воздействия агрессивной среды путем нанесения покрытий. [21]
Металл будет находиться в устойчивом пассивном состоянии при потенциале Еплг - - силе тока / плес - Другим принципиально отличным методом защиты в этих условиях является увеличение анодной поляризации путем введения в раствор анодных замедлителей, способствующих пассивирующей адсорбции, или легирование элементами, повышающими перенапряжение анодного процесса ( фиг. При этом резко снижается величина критического анодного тока. Этот эффект может быть достигнут также за счет уменьшения температурь. [22]
Характер анодных кривых для каждой структурной составляющей и каждого физически неоднородного участка зависит от химического состава этих составляющих, кристаллической структуры, концентрации ионов водорода, температуры, природы и концентрации активаторов, природы и концентрации анодных замедлителей, внутренних напряжений и приложенных внешних напряжений. [23]
Специфическая роль растворов также не находила отражения в общей структурной коррозии металлов, а между тем на особенности структурной коррозии большое влияние оказывают присутствующие в растворе окислительно-восстановительные системы, поверхностно-активные вещества, концентрация водородных ионов Известно, например, что при недостатке анодных замедлителей может возникнуть интенсивная язвенная коррозия, точно такое же явление может наблюдаться п в условиях неполной пассивности. Явления пассивности п перенассивации металлов должны быть учтены в общей теории структурной коррозии. Высокая степень чистоты обработки поверхности сплавов, достигаемая при химическом и электрохимическом полировании и фрезеровании должна быть также увязана е общей теорией структурной коррозии. [24]
По характеру своего действия различаются анодные и катодные замедлители. Анодные замедлители, например хромовокислые и двухромовокислые соли, способствуют образованию на анодных участках нерастворимых продуктов коррозии. Катодные замедлители, например некоторые органические вещества - желатина, клей, крахмал и др., образуют пленки на катодных участках поверхности металла. Действие их особенно эффективно в кислых средах. [25]
Анодные замедлители при введении их в коррозионную среду полностью подавляют коррозионный процесс, однако при недостаточном количестве ингибитора в среде возникает опасность увеличения интенсивности коррозии на отдельных участках поверхности металла. Поэтому анодные замедлители, добавленные в недостаточных количествах, весьма опасны, и надежной защиты можно достигнуть только при добавлении такого количества ингибитора, которое обеспечит полное прекращение коррозии. [26]
Замедлители коррозии подразделяются на две категории: анодные и катодные. К анодным замедлителям надо отнести соединения, способствующие пассивированию стали, например, NaNO2, K2Cr2O7, ( КаРОз) в ( их применение будет подробно описано в гл. Все замедлители анодного типа, добавленные в недостаточном количестве, сильно увеличивают местную коррозию, так как площадь анодных участков сокращается, а площадь катодных участков, которая определяет общий уровень коррозии, остается неизменной или даже может несколько возрастать. В противоположность анодным замедлителям концентрация катодных замедлителей не оказывает существенного влияния на коррозию. [27]
Замедлители коррозии подразделяются на две категории: анодные и катодные. К анодным замедлителям необходимо отнести соединения, которые способны снижать площадь анодных участков вследствие образования пленок из окисла металла или нерастворимой соли его. [28]
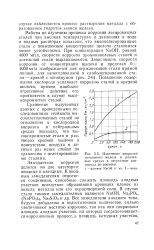 |
Изменение коррозии котельного железа в различных средах в отсутствие кислорода во времени. [29] |
Замедлители коррозии делятся на две категории: анодные и катодные. К анодным замедлителям относятся соединения, способные снижать площадь анодных участков вследствие образования кроющих пленок из окисла металла или его нерастворимой соли. [30]
Страницы: 1 2 3 4