Потенциал - хлорсеребряный электрод
Cтраница 2
Ввиду чрезвычайно малой растворимости AgQ потенциал хлорсеребряного электрода имеет положительный знак по отношению к нормальному водородному электроду. [16]
На рис. I приведены кривые зависимости потенциала хлорсеребряного электрода от концентрации хлорид-иона, рассчитанные теоретически и по-лучечнн практически. [17]
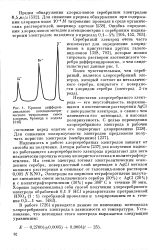 |
Кривая дифференциального потенциометри-ческого титрования смеси хлорида, бромида и иодида. [18] |
В работе [726] приводятся данные по изменению потенциала хлорсеребряного электрода в зависимости от температуры. [19]
Наличие хлоридного аниона в мембранной фазе должно обеспечить стабильный во времени потенциал хлорсеребряного электрода, а проведенное нами исследование пленочной мембраны такого же состава показало, что двукратного избытка валиномицина и тетрафенилбората калия над хлоридом тетрадециламмония достаточно для того, чтобы избежать влияния анионооб-менника на калиевую функцию. Хлоридный анион не липофилен, но CDB-ды, в которых должен работать миниатюрный калиевый ИСЭ, отличаются высокой концентрацией хлоридов при низком содержании других анионов. Поэтому можно надеяться, что скорость вымывания хлоркдны: -: иг - нов из мембраны не будет превышать скорость вымывание тетгадетдл-аммония и, следовательно, будет мала. Исследование подученных электродов с твердым контактом показало, что по пределам функ: шонир - вания, крутизне и селективности они не уступают электродам с внутренним водным раствором. [20]
Кроме того, в растворе не должны находиться вещества, искажающие потенциал хлорсеребряного электрода. Однако экспериментальные трудности, связанные с водородным электродом, могут быть устранены, путем замены последнего стеклянным электродом. [21]
Если концентрация хлор-ионов в исследуемом растворе строго постоянна, то в трубку втягивают испытуемый раствор и определяют потенциал хлорсеребряного электрода 3, сравнивая его с каломельным или водородным. [22]
Электропроводно-удельное электрическое сопротивление в зависимости от применяемого состава равно 100 - 1000 Ом - см. Осуществляет протекторную защиту - первоначальный потенциал относительно хлорсеребряного электрода составляет минус 0 85 - 0 95 В. Для реализации эффекта протекторной защиты рекомендуется наносить покрытие ЦВЭС на всю поверхность резервуара, включая днище, стенку и кровлю. Покрытие не накапливает статического электричества; не образует искр при ударе о посторонние предметы. Прочность покрытия на растяжение идентична прочности защищаемого металла, в результате чего сохраняется сплошность покрытия при деформациях резервуаров в процессе эксплуатации. Покрытие не горючее, содержит в своем составе 90 - 95 % металлического цинка. Покрытие экологически безопасно и ремонтопригодно. Поврежденные места зачищаются, обезжириваются и закрашиваются. [23]
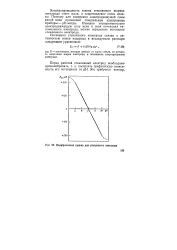 |
Калибровочная кррая для стеклянного электрода. [24] |
К - постоянная, которая зависит от сорта стекла, из которо: го изготовлен шарик электрода, и потенциала хлорсеребряного электрода. [25]
Исследуемый раствор должен содержать ион хлора в количестве, известном с точностью до 1 %, если необходимо иметь точность в несколько тысячных единицы р ( ан а) - Кроме того, в растворе не должны находиться вещества, искажающие потенциал хлорсеребряного электрода. Однако экспериментальные трудности, связанные с водородным электродом, могут быть устранены, путем замены последнего стеклянным электродом. [26]
Электропроводно-уделмюе электрическое сопротивление в зависимости от применяемого состава равно 100 - 1000 Омхм. Осуществляет протекторную защиту - первоначальный потенциал относительно хлорсеребряного электрода составляет минус 0 85 - 0 95 В. Для реализации эффекта протекторной защиты рекомендуется наносить покрытие ЦВЭС на всю поверхность резервуара, включая днище, стенку и кровлю. Покрытие не накапливает статического электричества; не образует искр при ударе о посторонние предметы. Прочность покрытия на растяжение идентична прочности защищаемого металла, в результате чего сохраняется сплошность покрытия при деформациях резервуаров в процессе эксплуатации. Покрытие не горючее, содержит в своем составе 90 - 95 % металлического цинка. Покрытие экологически безопасно и ремонтопригодно. Поврежденные места зачищаются, обезжириваются и закрашиваются. [27]
При погружении электродов в измерительную среду элементарный хлор восстанавливается на индикаторном электроде. Процесс восстановления происходит при постоянном потенциале, близком к потенциалу хлорсеребряного электрода. Возникающий в результате восстановления ток прямо пропорционален концентрации хлора в воде. [28]
В качестве электродов сравнения наиболее распространен хлорсеребряный электрод ( Ag, AgCl / KCl), который изготовляют электролитическим нанесением хлорида серебра на серебряную проволочку. Электрод погружают в раствор хлорида калия, который находится в сосудах, связанных солевым мостиком с анализируемым раствором. Потенциал хлорсеребряного электрода постоянен и не зависит от состава анализируемого раствора. Постоянство потенциала электрода сравнения достигается поддержанием в контактирующем внутреннем растворе постоянной концентрации веществ, на которые реагирует электрод. [29]
Хлорсеребряный электрод обычно изготавливают из серебряной проволоки, которую путем анодной обработки в хлоридном растворе покрывают тонким слоем хлорида серебра. Вместо серебряной проволоки иногда используют платиновую проволоку, электролитически покрытую серебром. Потенциал хлорсеребряного электрода является линейной функцией логарифма активности хлорид-ионов в растворе. [30]
Страницы: 1 2 3