Необратимый потенциал
Cтраница 2
 |
Стандартные потенциалы металлов. [16] |
В этих случаях устанавливаются стационарные или необратимые значения потенциалов. Необратимые потенциалы не могут быть отнесены к прямой и обратной реакциям одного и того же процесса и их нельзя вычислить по уравнению Нернста. [17]
Добавки ПАВ к электролиту существенно изменяют наводо-роживание стали, увеличивают пластичность и препятствуют коррозии. Введение ПАВ позволяет сблизить необратимые потенциалы выделения металлов. Этим пользуются для электрохимического изготовления сплавов. Адсорбцию промежуточных веществ и продуктов электрохимических реакций следует учитывать и з технологии электросинтеза. Для изучения адсорбции применяют электрокапиллярные измерения и определения дифференциальной емкости двойного слоя. Последний метод пригоден и для изучения адсорбции ПАВ на твердых электродах. [18]
В условиях эксплуатации металл обычно находится в растворе чужеродных ионов. В этом случае также возможно установление обратимых и необратимых потенциалов. [19]
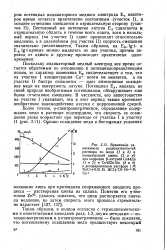
Поскольку индикаторный медный электрод все время остается обратимым по отношению к потенциалопределяющим ионам, то характер изменения Еи свидетельствует о том, что на участке I концентрация Си почти не меняется, а на участке II быстро снижается - идет интенсивное осаждение меди-на поверхность латуни. Потенциал Ед, являясь по своей природе необратимым потенциалом, обнаруживает еще более отчетливое смещение. В частности, его непостоянство на участке I указывает, что в-этот период также протекает необратимое взаимодействие латуни с коррозионной средой. [21]
В условиях эксплуатации металл обычно находится в растворе чужеродных ионов. В этом случае также возможно установление как обратимых, так и необратимых потенциалов. [22]
 |
Схема электрохимического процес - на анодных участках ПО ре-са коррозии акции ( 1. процесса перехо. [23] |
Как следует из уравнений ( 1) и ( 2) и схемы, приведенной на рис. 1, в случае электрохимической коррозии анодная реакция обеспечивается ионизацией атомов металла, подвергнутого коррозии, а катодная - разрядом ионов восстановителя. В результате деполяризующего действия восстановителя ( деполяризатора D) на металле через некоторое время устанавливается определенный необратимый потенциал, соответствующий равенству сумм скоростей анодных и катодных реакций, называемый стационарным потенциалом металла. Стационарный потенциал металла зависит от конкретных условий, в которых протекает процесс коррозии, и определяется экспериментально. [24]
Если в процессе взаимодействия металла и электролита участвуют не только ионы данного металла, но и чужеродные ионы и атомы, то возникающий на границе раздела фаз потенциал называется неравновесным, или необратимым. При этом анодный процесс обусловлен обменом собственных ионов металла, а катодный - другими ионами или молекулами, присутствующими в электролите. Значения необратимых потенциалов определяют опытным путем, так как их нельзя рассчитать по уравнению Нернста. [25]
Такой потенциал называется необратимым электродным потенциалом. Величина его определяется скоростью протекания электродных процессов и не может быть рассчитана термодинамически. Постоянное во времени значение необратимого потенциала рс называется стационарным или потенциалом коррозии. [26]
На их величину влияют различные факторы. По данным Г. В. Акимова, на величину необратимых потенциалов влияют: химическая природа металлов - 4 В, состояние поверхности металла - десятые вольта, адсорбция атомов и молекул - сотые и десятые вольта, механические напряжения - до сотых вольта, химическая природа и концентрация раствора - десятые вольта и вольты, изменение температуры на 10 С - сотые вольта. [27]
Страницы: 1 2