Фактический потенциал
Cтраница 1
Фактический потенциал в точке Q, создаваемый зарядом в точке Р и наводимыми им зарядами на s, равен / rp9 GpQ, где rpQ - расстояние от Рдоф. [1]
Фактический потенциал анода вследствие перенапряжения выделения хлора всегда больше теоретического и зависит от материала анода, плотности тока, концентрации NaCl в растворе и температуры - С повышением плотности тока перенапряжение увеличивается и соответственно растет потенциал анода. Увеличение концентрации NaCl и повышение температуры электролиза приводят к снижению потенциала анода. [2]
 |
К термодинамическому выводу 1С. [3] |
Поэтому замена фактического потенциала на иной ничего не меняет. Между тем если под понимается новое, фиктивное значение напряженности электрического поля, соответствующее равенству потенциалов с обех сторон, то после такой замены уравнение (VII.45) оказывается приложимым. При таком применении формула (VII.45) и п.с.м. верны всегда. [4]
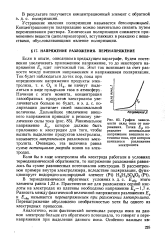 |
График зависимости силы тока от напряжения. Точка Ер определяет минимальное напряжение внешнего источника тока, при котором начинается разложение электролита. [5] |
Аналогично, если фактический потенциал разряда иона на данном электроде больше его обратимого потенциала, то говорят о перенапряжении при выделении данного иона. [6]
Перенапряжением называется разность между фактическим потенциалом разряда ионов при электролизе и обратимым значением потенциала для состояния равновесия и объясняется трудностью удаления ионов с некоторых электродов. Например, для выделения газообразных веществ - водорода, кислорода и др. - на цинке, свинце и особенно на ртути требуется более высокое напряжение, чем на платиновых электродах. [7]
КОНКУРЕНТНЫЙ СТАТУС ФИРМЫ - расчетный показатель, в котором сравниваются уровень и оптимум инвестиций с их критической точкой, фактический потенциал сопоставляется с оптимальным, а действующая стратегия - с оптимальной; разработана шкала оценки результата расчета показателя. [8]
В частном - случае, когда речь идет о перенапряжении при выделении водорода, величина TJ соответствует разности между фактическим потенциалом катода, на котором выделяется водород, и потенциалом обратимого водородного электрода в том же растворе. [9]
Допущение постоянства потенциала Фе на внешнем контуре может быть также опущено, если в уравнениях ( 8) и ( 11) Фе заменить усредненной величиной фактического потенциала на внешнем контуре. Этот вывод можно получить путем, совершенно аналогичным тому, что был выведен в гл. Ряд Фурье, который был использован для последнего, заменяется в данном случае соответствующими функциями - сферическими гармониками-полярных и азимутальных углов в и ( см. Byerly, гл. [10]
В действительности потенциал электрода, необходимый для разряда иона, значительно больше теоретического обратимого потенциала, определяемого по приведенным формулам. Величина фактического потенциала электрода зависит от материала электрода, плотности тока и температуры. Разность между величинами теоретического ( обратимого) электродного потенциала и действительного электродного потенциала называется перенапряжением. [11]
Выделение кислорода на нерастворимом аноде обычно наступает при потенциале более положительном, чем равновесный потенциал. Разница между фактическим потенциалом выделения кислорода и его равновесным значением называется перенапряжением кислорода. [12]
Однако многие исследователи считают, что пассивирующий окисел, если он существует в действительности, должен обладать какими-то особыми свойствами. Основывается этот взгляд на сопоставлении расчетных потенциалов образования окислов из металла и воды с фактическими потенциалами пассивирования металла. [13]
Однако многие исследователи считают, что пассивирующий окисел, если он существует в действительности, должен обладать какими-то особыми свойствами. Этот взгляд основан на сопоставлении расчетных потенциалов образования окислов из металла и воды с фактическими потенциалами пассивирования металла. Наибольшее количество таких сопоставлений проводилось и проводится для железа. [14]
Существенное значение для процесса электролиза имеет перенапряжение, представляющее разность между потенциалом разряда иона в данных условиях ( фактический потенциал) и равновесным потенциалом, то есть потенциалом неполяризованного ( неработающего) электрода. Перенапряжение является следствием концентрационной, электрохимической и химической поляризации и увеличивает потенциал разряда ионов: катодный в положительную сторону, анодный - в отрицательную сторону ( ф-ла 21.3), что может существенно изменить картину электролиза. [15]
Страницы: 1 2