Положительный окислительно-восстановительный потенциал
Cтраница 1
Положительный окислительно-восстановительный потенциал отвечает переходу в более устойчивое состояние, отрицательный - переходу в менее устойчивое состояние. Устойчивость трехвалентного состояния быстро возрастает от урана к америцию. Для кюрия вообще неизвестно никаких других состояний, кроме трехвалентного. Этот факт особенно важен для определения структуры седьмого периода системы Менделеева. Поэтому лютеций ( 4 / H5d6s2) и гадолиний ( 4 / 75dGs2) обладают особо устойчивой трехвалентно-стью. [1]
Положительный окислительно-восстановительный потенциал отвечает переходу в более устойчивое состояние, отрицательный - переходу в менее устойчивое состояние. Устойчивость трехвалентного состояния быстро возрастает от урана к америцию. Для кюрия вообще неизвестно никаких других состояний, кроме трехвалентного. Этот факт особенно важен для определения структуры седьмого периода системы Менделеева. Поэтому лютеций ( 4 / 145d6s3) и гадолиний ( 4 / 75d6s2) обладают особо устойчивой трехвалент-ностью. [2]
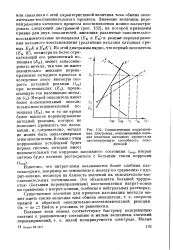 |
Схематическая коррозионная диаграмма, показывающая влияние кинетики катодного процесса на пассивирующую способность окислителей. [3] |
Второй окислитель имеет более положительный окислительно-восстановительный потенциал ( Ек), но в то; же время более высокое перенапряжение катодной реакции, которое не позволяет превысить ток пассивации, и, следователно, металл не может быть запассивирован этим окислителем. [4]
Это хорошо объясняется тем, что о-диоксибензол обладает слишком положительным окислительно-восстановительным потенциалом, чтобы гидрировать метиленовый голубой. [5]
На каждом этапе электрон передается акцептору, обладающему более высоким положительным окислительно-восстановительным потенциалом, и теряет при этом часть избыточной свободной энергии. Так как система переносчиков в трансаортной цепи электронов сопряжена с ферментными системами, катализирующими процесс фосфорилирования, то часть освобождаемой энергии превращается в энергию пирофосфатной связи АТФ. [6]
Причиной этого явления считают образование в средах с весьма положительным окислительно-восстановительным потенциалом оксидов металлов высшей валентности, хорошо растворимых в данной среде. [7]
Процесс обратного транспорта электронов требует энергии, и часть молекул АТФ, получаемых за счет окислительного фосфорилирования на конечном этапе дыхательной цепи, тратится для образования восстановителя. Окисление соединений с положительным окислительно-восстановительным потенциалом происходит, таким образом, без участия флавопротеинов и хино-нов. Эти переносчики функционируют только в процессе обратного переноса электронов. [9]
Биохимики за систему с большим положительным окислительно-восстановительным потенциалом принимают более сильный окислитель. [10]
Однако анодная поляризация при смещении потенциала положительное стационарного значения более чем на 0 2 В приводит к перепассивации рения ( благодаря образованию растворимых оксидов высшей валентности) и легкому анодному растворению рения. В азотной кислоте, где с самого начала устанавливается значительный положительный окислительно-восстановительный потенциал даже без анодной поляризации рений быстро растворяется. [11]
Известно много органических соединений, образующих обратимые окислительно-восстановительные системы с вполне устойчивыми окислительно-восстановительными потенциалами. Восстановленная форма такой системы, взаимодействующая с системой, имеющей более положительный окислительно-восстановительный потенциал, окисляется, а окисленная форма, взаимодействуя с системой, имеющей меньший окислительно-восстановительный потенциал, восстанавливается. Обычно в этих системах восстановленная форма бесцветна, а окисленная ярко окрашена. Подбирая такое органическое соединение, которое окисляется при определенном окислительно-восстановительном потенциале, можно наблюдать резкое изменение окраски системы. Это изменение окраски указывает на наличие в системе определенного окислительно-восстановительного потенциала, а тем самым и на наличие компонентов, обусловливающих этот потенциал. [12]
Автотрофные бактерии, окисляющие аммиак, нитрит, соединения серы или железо, находятся в энергетическом отношении в крайне невыгодных условиях. Их субстраты обладают сильно положительным окислительно-восстановительным потенциалом. Окисление названных выше неорганических субстратов не может быть прямо связано с восстановлением NAD. Однако NADH2 необходим для восстановления СО2 в рибулозобисфосфатном цикле. Судя по некоторым экспериментальным данным, электроны, освобождающиеся при окислении упомянутых неорганических субстратов, поступают в дыхательную цепь на уровне цитохрома с или цитохрома а. Поскольку фосфорилирование при этом может происходить лишь на одном-единственном этапе окисления, выигрыш в энергии соответственно невелик. Часть этой энергии затрачивается на то, чтобы оттеснить электроны, поступающие на участок цитохромов, по дыхательной цепи назад, на уровень пиридиннуклеотидов, и восстановить последние. [13]
Гидроксифенотиазин, получаемый осернением 4-гидроксиди-фениламина, легко окисляется с образованием красного ЗЯ-фено-тиазинона-3 ( фенотиазона) ( 224) и регенерируется из продукта окисления при действии восстановителей, например цинка в уксусной кислоте. Эти соединения находятся приблизительно в таких же отношениях, как фенотиазин, его катион-радикал, феназатиониевые ионы и 5-оксид. Фенотиазоны, в частности, имеющие более положительные окислительно-восстановительные потенциалы ( например, нитро - и 1-галогенфенотиазоны), присоединяют хлороводородную или бромоводородную кислоту к хинониминному циклу, превращаясь в 2 - и 4-галоген - З - гидроксифенотиазины. [14]
В пробирку с хромитом натрия, полученным в опыте 2, прибавьте 1 - 2 капли раствора щелочи и 3 - 5 капель 3 / 6-ного раствора перо-ксида - водорода. Нагрейте смесь на водяной бане или очень осторожно пламенем горелки до перехода зеленой окраски хромита в желтую, что указывает на образование в растворе хромата натрия. На основании данного опыта решите вопрос: Н2О2 или хромат-ион СгО имеет более положительный окислительно-восстановительный потенциал. [15]
Страницы: 1 2
