Ионизационный потенциал - элемент
Cтраница 1
Ионизационные потенциалы элементов, соответствующие отделению последнего валентного электрона или всех внешних электронов, а также система электроотрицательностей, по Полингу и по Горди, количественно подтверждают правомерность выделения третьих подгрупп и смещений в рядах аналогов. [1]
Полный ионизационный потенциал элементов главных подгрупп тем меньше, чем больше радиус атома и чем меньше электронов в его внешнем слое, иначе говоря, чем ниже и чем левее расположен элемент в периодической таблице. [2]
Ионизационным потенциалом элемента называют силу, которую необходимо приложить к нейтральному атому для отрыва с внеш. Эту величину выражают в вольтах. При отрыве электрона о-т нейтрального атома затрачивается работа, равная произведению заряда электрона на ионизационный потенциал. Эта работа выражается в электрон-вольтах. [3]
Ионизационным потенциалом элемента называют силу, которую необходимо приложить к нейтральному атому для отрыва с внешнего электронного уровня одного электрона. Эту величину выражают в вольтах. При отрыве электрона от нейтрального атома затрачивается работа, равная произведению заряда электрона на ионизационный потенциал. Эта работа выражается в электрон-вольтах. [4]
Из рассмотрения ионизационных потенциалов элементов и их сравнения с потенциалами галогенов следует, что у Не и Ne они даже выше, чем у F; у остальных элементов группы ниже потенциала F, а у Хе даже ниже потенциала хлора. Соответственно можно ожидать, что, по крайней мере, некоторые из газов не должны быть абсолютно инертными и способны, при благоприятных условиях вступать в реакции, например, с фтором. При этом реакшюнноспо-собность элементов подгруппы должна нарастать от Не к Хе. [5]
Рассмотрение затруднено недостаточной точностью определения ионизационных потенциалов элементов и разнообразием кристаллических структур окислов элементов левой части большого периода. [6]
На рис. 24 нанесены известные из спектроскопических данных ионизационные потенциалы элементов; они определяют энергии связи электронов, добавляемых при переходе от каждого элемента к следующему. [7]
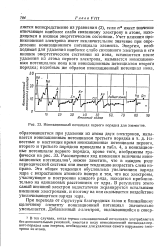 |
Ионизационный потенциал первого порядка для элементов. [8] |
Учет влияния проникновения электрона имеет исключительное значение при определении ионизационного потенциала элемента. [9]
 |
Энергии присоединения электрона ( сродство к электрону Е, эв, по. [10] |
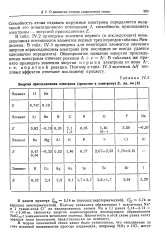
В табл. IV2 приведены значения первого ( и последующих) ионизационных потенциалов элементов первых трех периодов таблицы Менделеева. Поэтому в табл. IV.3 значения АЯ тепловых эффектов отвечают последнему процессу. [11]
Четвертые потенциалы ионизации не измерялись для элементов после церия [16] и их изменение для более тяжелых лантанидов должно основываться на имеющихся значениях ионизационных потенциалов элементов других групп периодической системы. [12]
Получаемые таким образом величины энергии ионизации близки к опытным данным. Полный ионизационный потенциал элементов главных подгрупп тем меньше, чем больше радиус атома и чем меньше электронов в его внешней оболочке, иначе говоря - чем ниже и чем левее расположен элемент в развернутой периодической таблице. [13]
Малая часть образовавшихся таким путем ионов ( - 10 - 4) захватывается в режим статистического ускорения. При этом важно, что ионизационный потенциал элементов, составляющих аномальную компоненту, выше, чем у других элементов, также, по-видимому, имеющихся в межзвездной среде, таких как С, Mg, Si, Fe. Последние ионизуются уже в межзвездной среде или на периферии солнечного ветра и не могут в значительных количествах проникать в глубь Солнечной системы. [14]
Неправильно было бы предполагать, что свойства элементов ( и их соединений) в подгруппах всегда монотонно меняются с порядковым номером. Отложим, например, по оси ординат сумму первых четырех ионизационных потенциалов элементов IV группы, а по оси абсцисс - их порядковый номер. Из полученного графика ( рис. 30) видно, что точки для атомов С, Si, Ti, Zr и Hf могут быть соединены плавной кривой. [15]
Страницы: 1 2