Кислородный потенциал
Cтраница 2
Фактором, влияющим на окислительно-восстановительный процесс при определенных концентрациях исследуемого элемента является кислородный потенциал среды ( ИГ In PoJ - Равновесие между металл - оксид металла при определенном кислородном потенциале резко изменяется с изменением температуры. Любой металлический оксид может быть восстановлен при увеличении температуры, но максимальная температура спекания определяется в основном рабочей температурой серийно выпускаемых промышленностью печей. [16]
В отличие от q a3 ( p, ( pV, 1 со2 ( 1 45 В) выше кислородного потенциала, поэтому для окисления Со2 в Со3 требуется более сильный окислитель, чем кислород воздуха. Чаще всего для этой цели используют газообразный хлор. [17]
 |
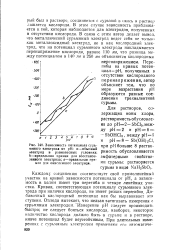
Кислородный потенциал атмосфер спекания. [18] |
Фактором, влияющим на окислительно-восстановительный процесс при определенных концентрациях исследуемого элемента является кислородный потенциал среды ( ИГ In PoJ - Равновесие между металл - оксид металла при определенном кислородном потенциале резко изменяется с изменением температуры. Любой металлический оксид может быть восстановлен при увеличении температуры, но максимальная температура спекания определяется в основном рабочей температурой серийно выпускаемых промышленностью печей. [19]
Чтобы поддерживать заданный ( низкий) потенциал кислорода в реакционной камере при температуре Т, часто удобно пропускать поток СО и СО2 с определенным их соотношением, отвечающим требуемому кислородному потенциалу. Таким образом, в эксперименте часто оказывается важным контроль выпадения углерода. [20]
Кривая, соответствующая потенциалу сурьмяного электрода при наличии кислорода, не имеет резких перегибов. Добавочный кислородный потенциал как бы выравнивает эти ступени. Отсюда вытекает, что нельзя затягивать измерения с сурьмяным электродом. Измерение, рН следует производить быстро; не следует бояться кислорода, наоборот, некоторое количество кислорода должно быть в сурьме и в растворе, иначе потенциал будет неустойчивым. При длительных измерениях с сурьмяным электродом применяют его автоматическую зачистку, не прерывая измерения, с тем чтобы ускорить установление потенциала. [21]
Повышение кислородного потенциала в шлаке и расплаве; высокая реакционная способность [ Р ] и СаО ( активный шлак); суммарная реакция дефосфорацин экзотер-мична, а с ростом температуры равновесие сдвигается в сторону повышения содержания Р, поэтому дефосфорацию проводят при низких температурах. [22]
В области горения кокса у фурм образуется газовая фаза, отличающаяся по своим свойствам от газов во всем остальном объеме доменной печи. Она имеет повышенный кислородный потенциал и определяет границы окислительной зоны в горне доменной печи. [23]
Потенциалы взяты относительно стационарного кислородного потенциала. [24]
Представляя теплотворную способность в виде произведения кислородного потенциала Ккас, на расход кислорода О0, Коновалов пришел к выводу, что непостоянство характеристики Кки. Прочие же соединения дают значения Кнас отклоняющиеся от этой нормы вверх и вниз. [25]
У металлов, линии которых находятся в нижней части диаграммы, наиболее стабильные, трудно разлагающиеся оксиды. Как видно из диаграммы, для перевода этих оксидов в металлическое состояние необходим очень низкий кислородный потенциал. [26]
Каждому соединению соответствует свой прямолинейный участок на кривой зависимости потенциала от рН, а зависимость в целом имеет три перегиба и четыре линейных участка. Кривая, соответствующая потенциалу сурьмяного электрода при наличии кислорода, не имеет резких перегибов. Добавочный кислородный потенциал как бы выравнивает эти ступени. Отсюда вытекает, что нельзя затягивать измерения с сурьмяным электродом. Измерение рН следует производить быстро; не следует бояться кислорода, наоборот, некоторое количество кислорода должно быть в сурьме и в растворе, иначе потенциал будет неустойчивым. [28]
Потенциал без нагрузки и при катодной нагрузке, как и для водородных электродов, определялся по отношению к насыщенному каломельному электроду; промежуточный сосуд с КС1 служил для исключения диффузионных потенциалов. Измерение кислородного потенциала производилось через усилитель постоянного тока ( фирма Кник, Берлин), который при входном сопротивлении более 1010 ом позволяет производить измерение практические без отбора тока. В качестве вспомогательных электродов применялись никелевые листы или Ni-ДСК-электроды, на которых анодно выделялся кислород, катодно восстановленный на серебряных ДСК-электродах при помощи внешнего источника тока. [29]
Имеются и другие трудности. Некоторые металлы, особенно платина, палладий и родий, могут сильно растворять кислород, что может привести к гистерезису, легко заметному на кривых заряжения. Многие металлы, даже золото, при кислородном потенциале имеют тенденцию к окислению. Поверхностные окислы ответственны также за пассивационные характеристики, например, сплавов двухвалентного железа. [30]
Страницы: 1 2 3