Электродный потенциал - образец
Cтраница 2
Повторное нагружение образца вызывает заметный рост разности потенциалов пары. Этот рост обусловливается главным образом более быстрым разблагораживанием электродного потенциала образца, испытывающего знакопеременные напряжения. Ход кривой силы тока в общем отражает изменение разности потенциалов исследуемой нары. [16]
Находят степень анодного контроля ( в процентах) при коррозии напряженного металла в электролитах. Для этого используют последнее ( перед обрывом образца) значение электродного потенциала образца. [17]
Однако наличие трещин не обязательно сопровождается смещением электродного потенциала в отрицательную сторону. Как показывает кривая / / / ( см. рис. 72), электродный потенциал образцов, испытанных при напряжении 10 кгс / мм2, начинает отличаться от потенциала ненагруженных образцов только перед окончательным разрушением. Глубина же образующейся к этому моменту ( точка 8) трещины может достигать 4 мм при диаметре рабочей части образца 9 5 мм. Таким образом, рост трещины происходит при практически неизменном электродном потенциале. Это можно объяснить тем, что при низком уровне напряжения трещина развивается сравнительно медленно и появляющаяся в процессе ее роста ювенильная поверхность в условиях интенсивного перемешивания раствора успевает запас-сивироваться. [18]
Ускоренный приближенный электрохимический метод испытания на точечную коррозию состоит в том, что образец стали поляризуют анодно от внешнего источника постоянного тока и одновременно измеряют его электродный потенциал. При достижении некоторого значения потенциала защитная пленка на образце подвергается точечному разрушению, вследствие чего значение электродного потенциала образца практически не меняется с увеличением поляризующего тока. Достигнутое при анодной поляризации постоянное значение потенциала называется потенциалом пробивания. Потенциал пробивания может быть использован в качестве количественной характеристики устойчивости пассивного состояния коррозионностойких сталей. [19]
Ускоренный электрохимический метод испытания на точечную коррозию состоит в том, что образец стали поляризуют анодно от внешнего источника постоянного тока и одновременно измеряют его электродный потенциал. При достижении некоторого значения потенциала защитная пленка на образце разрушается в одной или нескольких точках, вследствие чего значение электродного потенциала образца уменьшается. [20]
Основанием для этого были явления перехода осажденного коллоидного серебра при нагревании в новую форму со значительным выделением теплоты, равличный термический эффект растворения в ртути образцов серебра, полученных разными способами, различный удельный вес ( 10 42 - 10 51) образцов, полученных или обработанных различным образом, замедление при 77 расширения образцов серебра при нагревании, различная плотность и электродный потенциал образцов серебра, подвергнутых нагреванию в растворах различных солей. [21]
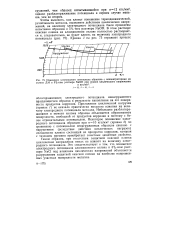 |
Изменение электродного потенциала образцов с концентраторами из сплава Д16 в 5 % - ном растворе NaOH при уровне циклического напряжения. [22] |
Приложение циклической нагрузки ( кривая 1) не оказало практически никакого влияния на величину электродного потенциала металла. Небольшое разблагораживание в момент излома образца объясняется образованием поверхности, свободной от продуктов коррозии и поэтому с более отрицательным потенциалом. Некоторое понижение электродного потенциала образцов при о10 кгс / мм2 ( кривая 2) по сравнению с потенциалом ненагруженных образцов связано с нарушением ( вследствие действия циклических нагрузок) сплошности пленки состоящей из продуктов коррозии, которая с течением времени приобретает заметные защитные свойства. Таким образом, при отсутствии защитной окисной пленки циклические напряжения никак не влияют на величину электродного потенциала. Это свидетельствует о том, что понижение электродного потенциала алюминиевого сплава в 3 % - ном растворе NaCl под влиянием циклических напряжений объясняется разрушением защитной окисной пленки на наиболее напряженных участках поверхности металла. [23]
Для стрел прогиба 3: 13 и 18 им они соответственно равны 530 - 545 567 мв. Разница в значениях электродных потенциалов образцов с различными стрелами прогиба не уменьшается со временем, а, наоборот, имеет определенную тенденцию к увеличению. [24]
Поддерживая электродный по-енциал испытуемого образца постоянным или регулируя его по шределенной программе, определяют результирующий коррозионный ок. Ток является мерой скорости коррозии, которую можно щределить также по потере массы. Поскольку скорость коррозии шсто сильно зависит от электродного потенциала образца, иногда гдобно вести коррозионное испытание в водном растворе при тотенциостатических условиях. [25]
Страницы: 1 2