Электродный потенциал - сплав
Cтраница 2
 |
Схема границ ( порогов устойчивости. [16] |
Коррозионная стойкость стали может быть повышена, если, во-первых, содержание углерода снизить до минимально возможного количества и, во-вторых, ввести легирующий элемент, образующий с железом твердые растворы, в таком количестве, при котором скачкообразно повысится электродный потенциал сплава. [17]
Прямого контакта между сплавами алюминия и магния лучше избегать, так как магний намного неблагороднее, чем алюминий, и в отличие от алюминия не образует активного защитного слоя. Сравнение электродных потенциалов сплавов магния дано в табл. 11.3 ( ср. [18]
Однако одной однородности сплавов еще недостаточно для получения высокой коррозионной стойкости. Необходимо, чтобы электродный потенциал сплава также был достаточно высоким. В противном случае возможна реакция обмена с катионами, находящимися в растворе. [20]
При взаимодействии на поверхности сплава растворов электролитов структурные составляющие корродируют со скоростями, которые зависят от их электрохимических свойств, состава коррозионной среды и величины электродного потенциала. В общем случае при данном электродном потенциале сплава скорости коррозии структурных составляющих различив. [21]
 |
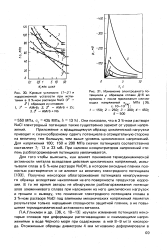
Потенциостатические кривые образцов из сплава ВТ14 при различном времени обновления поверхности в 0 5 н. кривые 7, /, 3, 3. и 1 0 н. ( кривые 2, 2., 4, 4 растворах NaCI. [22] |
После прекращения зачистки свежеобразованная поверхность быстро репассивирует. В первые 1 - 2 с электродный потенциал сплава резко сдвигается в положительную сторону на 200 - 400 мВ, а затем более плавно смещается до исходного значения. [23]
Для того чтобы иметь возможность более полно судить о процессах, происходящих при коррозии на поверхности металла, нами было изучено изменение потенциалов сплава во STf 0 00 от держания никеля. В 0 5 % - ном растворе wau электродный потенциал сплава с увеличением содержания в нем никеля закономерно облагораживается. [24]
Показано, что повышение СКР может быть достигнуто за счет локализации коррозионных поражений. Это явление возникает при смещении области потенциала пробоя до электродного потенциала сплава, что осуществляется путем добавления к раствору, содержащему пассиватор, активатора. [25]
Такое состояние приповерхностных слоев в процессе усталости обеспечивает контакт коррозионной среды с большими площадями металла, усиливает электрохимическую неоднородность участков поверхности, активирует коррозионные процессы, способствует проникновению коррозии вглубь металла. Действительно, проведенные авторами исследования по изучению влияния циклических напряжений на величину электродного потенциала сплава Д16 показали, что в процессе усталости происходит непрерывное изменение электрохимических свойств поверхности нагружаемого в коррозионной среде металла. [26]
Таким образом, если сплав обладает СКР, то потенциал пробоя относится к числу важнейших характеристик, определяющих скорость КР. Следовательно, для проведения ускоренных испытаний на СКР внешние факторы должны быть подобраны таким образом, чтобы электродный потенциал сплава находился в области потенциала пробоя. Наиболее просто это условие может быть выполнено путем подбора состава коррозионного раствора. Известно, что изменение соотношения концентраций пассиватора и активатора позволяет в широких пределах смещать потенциал пробоя. [27]
Получено некоторое облагораживание потенциала ненагруженного образца вследствие накопления на его поверхности продуктов коррозии. В то же время авторы не обнаружили разблагораживания потенциалов алюминиевого сплава при наложении на него циклических нагрузок и пришли к выводу, что понижение электродного потенциала сплава в 3 % - ном растворе NaCI под влиянием механических напряжений является результатом только нарушения сплошности защитной пленки, а не повышения термодинамической активности металла. [29]
 |
Зависимость скорости коррозии нержавеющей стали Х18Н10Т от концентрации при 50 С. [30] |
Страницы: 1 2 3