Указанный потенциал
Cтраница 2
В общем случае значения указанных потенциалов не тождественны. [16]
Так как сталь при указанных потенциалах находится в активном состоянии и корродирует по всей поверхности, эти условия не имеют большого значения для практики. [17]
Эти результаты показывают, что при указанных потенциалах, а также, по-видимому, и при несколько менее положительных потенциалах ( судя по неизменности наклона анодной поляризационной кривой) рений действительно переходит в раствор в виде ионов высшей валентности, окислы которых легко растворимы в воде и кислотах. Этим и определяется большая скорость анодного растворения рения при указанных потенциалах. [18]
Пользуясь языком синергетики, рискну утверждать, что указанный потенциал является решающим условием самоорганизации и саморазвития общества, условием его выживания и прогресса. [19]
При этом кривая зависимости выхода металла от потенциала катода имеет при указанном потенциале резкий максимум типа острого пика: при меньших потенциалах катода, как видно из изложенного выше, лантан еще не может разряжаться, а при немного более высоких потенциалах уже начинается настолько сильная конкуренция со стороны щелочного металла или водорода, что выход лантана резко падает. [20]
В присутствии золета ( III), которое также восстанавливается на электроде при указанном потенциале, ток повышается, но это не мешает определению конечной точки, если количество золота не слишком велико - не больше 15 - 20-кратного по отношению к рутению. Если золота больше, то оно одновременно с рутением восстанавливается гидрохиноном. Определению рутения этим методом мешают двухвалентное железо ( анодный ток окисления, компенсирующий катодный ток рутения) и иридий. Метод применим для определения 0 02 - 2 0 мг рутения. [21]
В присутствии золота ( III), которое также восстанавливается на электроде при указанном потенциале, ток повышается, но это не мешает определению конечной точки, если количество золота не слишком велико - не больше 15 - 20-кратного по отношению к рутению. Если золота больше, то оно одновременно с рутением восстанавливается гидрохиноном. Определению рутения этим методом мешают двухвалентное железо ( анодный ток окисления, компенсирующий катодный ток рутения) и иридий. Метод применим для определения 0 02 - 2 0 мг рутения. [22]
В присутствии золота ( III), которое также восстанавливается на электроде при указанном потенциале, ток повышается, но это не мешает определению конечной точки, если количество золота не слишком велико - не больше 15 - 20-кратного по отношению к рутению. Если золота больше, то оно одновременно с рутением восстанавливается гидрохиноном. [23]
Потенциалы, наблюдаемые при электролизе простых солей, по своим значениям близки к величинам указанных потенциалов. [24]
Объективным показателем того, что осадок металла снят, служит отсутствие тока в цепи при указанных потенциалах. Не следует проводить анодную поляризацию с целью очистки электрода при потенциалах, сильно ( например, на 0 8 - 1 0 в) отличающихся от нормального потенциала данной системы, так как в таком случае может начаться выделение кислорода, которое приведет к некоторому изменению поведения электрода при титровании. Не следует также очищать электрод электрохимическим способом в нейтральных фонах и в растворах, содержащих анионы, с которыми ионы растворяющегося металла способны давать осадки, так как в этом случае будут образовываться и осаждаться на поверхности электрода гидроокиси, окислы и другие малорастворимые вещества. В тех случаях, когда могут иметь место подобные явления, осадок металла следует удалять химическим путем. [25]
Тем не менее следует подчеркнуть, что в электроэнергетике возможности эксплуатационного персонала влиять на эффективность производства ограничены указанным потенциалом. Следовательно, эффективность деятельности машиностроителей, проектных, строительных и монтажных организаций в значительной мере предопределяет эффективность энергопроизводства на электростанциях и в сетевых предприятиях. [26]
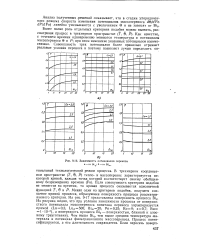 |
Зависимость потенциалов переноса, а - от Bi. 6-от Bim. [27] |
Как известно, с течением времени одновременно меняются температура и потенциалы массопереноса 6 и Я; при этом изменение указанных потенциалов взаимосвязано. [28]
В связи с тем, что скорость ионов в каждом трехсе-точном каскаде несколько возрастает от высокочастотного потенциала, кроме указанных потенциалов к каждому трехсеточному каскаду подается дополнительное напряжение смещения f / CM для обеспечения постоянства скорости регистрируемых ионов. [29]
Если железо ( II) присутствует вместе с восстановленным ( четырехвалентным) ванадием, то сперва титруют железо церием при указанном потенциале 0 9 в ( Нас. КЗ), причем кривая титрования имеет форму а, а когда сила тока перестанет уменьшаться ( признак того, что все железо оттитровано), изменяют потенциал индикаторного электрода ( платинового) на 0 5 в ( Нас. [30]
Страницы: 1 2 3 4