Замена - метил
Cтраница 1
Замена метила в карбамоильной группе на этил существенно не изменяет токсичности соединения, но с увеличением числа атомов углерода при азоте инсектицидная активность соединения уменьшается. При замене второго атома водорода при азоте на углеводородный радикал инсектицидность также снижается. При замене этого водорода на карбалкоксильный радикал или формильный остаток инсектицидность соединения существенно не снижается, но повышается токсичность для млекопитающих. Инсектицидными свойствами обладают также соединения, содержащие дипептидные группы, концевой карбоксил которых этерифицирован низшим спиртом. [1]
Замена метила ка другие алкильные группы R G-положе-нии хинолинового цикла не ведет к альтернированию физиологической активности. [2]
Если мостик состоит из 3 атомов углерода, то возможность пространственных препятствий сильно снижается и при замене метила на, водород область поглощения лежит в коротковолновой части спектра. Это обстоятельство подчеркивает специфичность систем, в которых ярко выражены пространственные затруднения. [3]
Наиболее вероятные места модификации - замена фенила ( СС группы) с выходом на ациклические или гетероциклические заместители, замена метила при атоме азота и фтора. [4]
В этом случаеso наблюдается замена метила на бром. Трансформация ускоряется при дестил-ляции, и то же самое имеет место с иодом. [5]
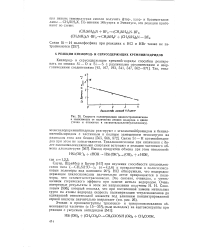 |
Скорость полимеризации циклотетрасялоксанои в зависимости от количества атомов водорода в цикле ( точка и относится к октаметилциклотетрасилоксану. [6] |
Сауер, Шрайбер и Бруэр [167] при изучении способности циклосилок-санов типа ( - CH3SiHO -) ( л 4 5 6) к превращению в полисилокса-новые полимеры под влиянием 20 % НС1 обнаружили, что водородсо-держащие циклосилоксаны значительно легче превращаются в полимеры, чем октаметилтетрасилоксан. Это связано, очевидно, с уменьшением стерического эффекта при замене метила водородом. [7]
Серией этих исследований была подтверждена концепция о пространственных затруднениях в N-метилметенах. У соединений, мостик которых состоит из единственного атома углерода, замена метила на водород приводит к возвращению обычного эффекта и смещает область поглощения в сторон более длинных волн. [8]
Оказалось, что суммарная энергия активации гидрогенолиза моноалкилциклопентанов с неразветвленными цепями мало отличается от энергии активации гидрогенолиза самого циклопентана. Если же определять энергии активации гидрогенолиза отдельных связей, то оказывается, что для связей, прилегающих к углеродному атому, несущему метальный заместитель, величина энергии активации на 2 - 2 5 ккал / моль больше, чем для остальных связей. При замене метила на алкил большего объема, например изопропил, от которого можно ожидать большего экранирующего эффекта но отношению к соседним связям кольца, разница достигает уже 7 9 ккал / моль. [9]
Страницы: 1