Аксиальный заместитель
Cтраница 1
Аксиальный заместитель при этом становится экваториальным, а экваториальный аксиальным. В результате конверсии кресло - кресло устанавливается равновесие, в котором экваториального изомера тем больше, чем больше заместитель. Поэтому, например, тпрещ-бутилциклогексан на 100 % представлен экваториальным конформером. Таким образом, большой заместитель фиксирует одну из форм кресла, и конверсия прекращается. [1]
Только аксиальный заместитель при р-углеродном атоме способен играть роль соседней группы в реакциях замещения соединений циклогексана ( ср. Примеры этого были недавно изучены Альтом и Бартоном ( Alt, Barton, 1954); 2 ( 3 - ( а) - бромхолестанол - За ( а) - ( ЬХХУ) при действии бромисто-водородной и уксусной кислот дает 2р ( а), За ( а) - дибромхолестан с промежуточным образованием иона бромония ( ср. Соответствующее диэква-ториальное соединение ( 2а - бромхолестанол - 3р -) нереакционно-способно. [2]
Любой аксиальный заместитель, отличный от водорода, вносит вклад в понижение стабильности конформации. [3]
Неустойчивость аксиальных заместителей ( например, X в XXIV) вызвана взаимным отталкиванием между X и двумя аксиальными атомами водорода с той же стороны кольца у С-3 и С-5. Экваториальный заместитель в XXIII не подвергается такому отталкиванию. [4]
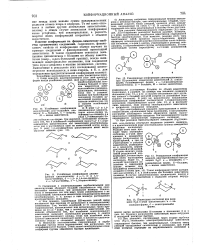
Изомер с тремя аксиальными заместителями по одну сторону кольца не способен к существованию подобно другим соединениям этого типа. Весьма вероятно, что даже в этих случаях изменены углы связей и торсионные углы отдельных фрагментов молекулы. Случаи обратного порядка стабильности очень редки. Бартон показал, что заместитель при С ( 2 в соединениях, диаксиально замещенных в 1 3-положениях, более стабилен в аксиальном положении, чем в экваториальном. Эта аномалия может быть проиллюстрирована некоторыми примерами стабилизации аксиального положения заместителей при Qi) и С ( 3) или благодаря образованию мостика, или благодаря действию других заместителей. Например, в 1 3-ангидриде циклогексан-1 2 3-трикарбоновой кислоты ( XI) свободная карбоксильная группа при атоме углерода С ( 2) более устойчива в аксиальном положении. [5]
Поскольку в монозамещенном циклогексане аксиальный заместитель X взаимодействует с двумя аксиальными атомами водорода, энергия взаимодействия одного атома водорода с группой X составляет 1 / 2 AG j ( как определено в гл. [6]
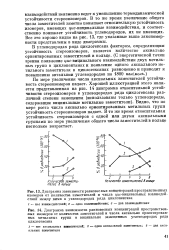
По мере увеличения числа аксиальных заместителей устойчивость стереоизомеров падает. Видно, что по мере роста числа аксиально ориентированных метальных групп устойчивость стереоизомеров падает. В то же время относительная устойчивость стереоизомеров с одной или двумя аксиальными группами по мере увеличения общего числа заместителей в кольце несколько возрастает. [8]
 |
Устойчивые конформации 2 В ряду 1 2 - и 1 4.| Переходные состояния при реакциях Sj 2 в ряду циклогексана. а - аксиальная форма, 6 - экваториальная форма. [9] |
То же самое относится к любым другим аксиальным заместителям, поэтому в общем случае аксиальная конформация менее устойчина, чем экваториальная, а разность энергии обеих конформаций возрастает с объемом заместителя. [10]
То же самое относится к любым другим аксиальным заместителям, поэтому в общем случае аксиальная конформация менее устойчива, чем экваториальная, а разность энергии обеих конформаций возрастает с объемом заместителя. [12]
Далее предстоит выяснить величину взаимодействия между аксиальным заместителем и кислородным атомом кольца. У такого атома отсутствует аксиальный атом водорода, имеющийся в цик-логексановом кольце. Известно, однако, о существовании взаимодействия, по крайней мере частичного, с парой электронов, образующей связь Н - О. Кроме того, кислородный атом кольца содержит на той же орбитали неподеленную пару электронов. Относительно взаимодействия последней имеются различные данные. Так, Арони и Лефевр [ 541 утверждают, что объем, занимаемый неподеленной парой электронов атома азота, превышает объем ковалентно связанного водородного атома ( разд. Аналогичной точки зрения придерживается Бартон [55], рассматривая неподеленную пару электронов карбаниона. Тем не менее имеющиеся в настоящее время сведения ( разд. Кажется, пока нет надежных данных, касающихся неподеленных электронных пар на атоме кислорода. Химия углеводов предоставляет лишь одну относящуюся к данному вопросу цифру. Так, известно [56], что разность свободных энергий между 1-фосфатами а-в-глюкозы и cc - D-галактозы составляет 0 7 ккал / молъ. Оба эти соединения различаются лишь расположением гидроксильной группы при G-4, аксиальной в случае галактозы. [13]
Как и в случае циклогексана, конформация с наименьшим числом аксиальных заместителей является наиболее устойчивой. При этом, чем больше объем заместителя, находящегося в аксиальном положении, тем менее стабильной оказывается данная кокформация. Наиболее объемистый заместитель в гексопиранозах - СН2ОН - группа, которая поэтому располагается обычно экваториально, что оказывает значительное влияние на конформацию соединения в целом. [14]
Атомы, расположенные в заднем нижнем левом октанте ( например, аксиальный заместитель при С ( 6)) и заднем верхнем правом октанте ( углерод С ( з и оба заместителя, связанные с ним), дают отрицательный вклад; заместители в дальнем нижнем правом октанте ( аксиальный заместитель при С ( 2) и в дальнем верхнем левом октанте ( углерод Сдо и два заместителя, связанные с ним) дают положительный вклад. Ни один из атомов, оказывающих существенное влияние, не расположен в этих октантах, и, следовательно, ими можно пренебречь. Суммируя вклады отдельных атомов, не лежащих в плоскостях ( которые частично гасят друг друга), определяют знак результирующего вклада, который одновременно представляет собой знак эффекта Коттона исследуемого вещества. [15]
Страницы: 1 2 3 4