Галогенный заместитель
Cтраница 1
Галогенные заместители, которые ослабляют основные свойства пиридина и незначительно дезактивируют пиридиновое кольцо к реакциям с электрофилами, действуют иначе - приводят к повышению концентрации непротонирован-ного пиридина в реакционной смеси. [1]
Как и в случае бензола, введение галогенных заместителей уменьшает основность моноолефинов. К сожалению, нет данных, которые позволили бы судить, вызывает ли этот эффект только атом галогена, связанный с углеродом при двойной связи С С, или также атом галогена, связанный с соседним насыщенным атомом углерода в олефине. [2]
Таким образом, метильная группа рассматривается так же, как галогенный заместитель. Хотя была выбрана определенная ориентация группы СН3 в проведенном рассмотрении, можно показать, что степень делокализации электронов между метильной группой и кольцом не зависит от ориентации группы. [3]
Описано хлорирование аллпльных групп в ССЦ при помощи некоторых N-хлор-ациланилидов с галогенными заместителями в ядре. РТ-Хлорсукцинимид применяют для аллилхлорирования только в некоторых, специальных случаях, например для получения 5-ялорметилурацила или 6-хлор-метил - 2-метилтиоурацила из 5-мвтилурацжла или 2 6 - дииетилти0урацила в кипящеьг СНС18 С добавкой 15 мол. [4]
Винилгалогениды образуют менее стабильные аддукты с иодом, чем соответствующие ал-кены, поскольку индуктивный эффект галогенных заместителей уменьшает способность молекул быть донорами л-электронов. [5]
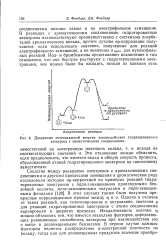 |
Диаграмма потенциальной энергии взаимодействия гидратированного электрона с ароматическими соединениями. [6] |
Это отклонение можно объяснить, если предположить, что имеется вклад в общую скорость процесса, обусловленный атакой гидратированного электрона по галогенному заместителю. [7]
Так, две алко-ксикарбонильные группы понижают рКа приблизительно до 13; рКа а-нитропиррола составляет 10 6; 2 4-динитропиррола 6 15; 2 5-динитропиррола 3 6, что указывает на более эффективное сопряжение электроноакцепторных а-заместителей с неподеленной электронной парой атома азота. Галогенные заместители также заметно повышают кислотность пирролов. [8]
Так, две алко-ксикарбонильные группы понижают рКа приблизительно до 13; рКа а-нитропиррола составляет 10 6; 2 4-динитропиррола 6 15; 2 5-динитропиррола 3 6, что указывает на более эффективное сопряжение электроноакцепторных а-заместптелей с неподелепной электронной парой атома азота. Галогенные заместители также заметно повышают кислотность пнрролов. [9]
Фенильные заместители ведут себя, как заместители со слабо выражен ными электроноакцепторными свойствами. Карбоксильные, карбомет-оксильные, ацетильные и галогенные заместители оттягивают электроны и значительно замедляют дейтерирование. Наоборот, метоксильные группы немного ускоряют, но все же слабее, чем алкильные. Итак, можно сделать вывод о том, что ферроцен поддается гораздо легче действию электроноак-цепторных заместителей, чемэлектронодонорных. Уменьшение реакционной способности атомов водорода 5-членных циклов в ходе электрофильного замещения под влиянием акцепторных заместителей наблюдается не только в случае дейтерообмена, но также и в других реакциях электрофильного замещения; ацетилирование и сульфирование производных ферроцена, несущих; электроноакцепторные заместители, такие, как ацетильные группы [17,18], карбометоксильные [17, 19, 20], бром [21], фенил [22], протекает труднее, чем для ферроцена; эти группы вступают главным образом в свободный цикл. [10]
Поэтому вполне может быть, что катализируемой кислотой енолизации карбоновой кислоты не происходит, но енолизация бромангидрида протекает. Это различие может быть объяснено тем, что мезомерия в карбоновой кислоте ( IX) уменьшает электрофильный характер карбоксильной группы; в бромангид-риде ( X) электрофильный характер увеличивается благодаря индуктивному влиянию галогенного заместителя. [11]
При этом вторичный атом водорода замещается хлором легче, чем первичный. Наличие гало-геппих ааместитслей затрудняет дальнейшее га доге встревание и притом особенно сильно у атома углерода, ужо имеющего галогеа. Но мере удаления от этого атома влияние галогенного заместителя ослабляется. Наличие двух или трех атомов хлора у одного и того же атома углерода препятствует дальнейшему свобо дно ра дика лъ-поьгу хлорирован то ЗОЙСГ2 таких соединений, как, например, хлороформ, тетра-хлорэтан или хлористый бензшшден. [12]
На примере галогенов отчетливо видно возрастание действия заместителя с ростом его электроотрицательности в случае, когда только один атом углерода отделяет его от изопропильной группы. Эффект резко уменьшается, если между заместителем и рассматриваемой связью появляется еще один атом углерода. Существует прямая связь этих данных с имеющимися в литературе другими величинами, характеризующими электроотрицательность галогенных заместителей. [13]
Незамещенные 2-галогенопирролы - соединения крайне нестабильные. Га-логенопирролы, а также 2-галогенопирролкетоны и эфиры 2-галогенопиррол-карбоновых кислот вполне устойчивы. Химические превращения с участием галогенопирролов наиболее легко идут при наличии электроноакцепторных заместителей у атома азота. Галогенопирролы подвергаются каталитическому гидрогенолизу, что позволяет использовать галогенные заместители в качестве блокирующих. [14]
В дальнейшем мембраны на основе арамидов получали из полностью ж-замещенных мономеров, в которых было просуль-фировано 10 % ароматических колец. Такие полимеры растворяются в ДМСО. Вначале считалось, что это обусловлено присутствием - NH-групп в основной цепи полимера. Однако, по данным работы [89], это, по-видимому, обусловлено тем, что ароматические кольца галогенируются по реакции электрофильного замещения. Объемность галогенных заместителей, в свою очередь, приводит к изменению типа водородной связи - от межмолекулярной к внутримолекулярной. Это обусловливает деформацию цепи и чередование средней величины межцепного смещения в поверхностной структуре мембраны. В результате возрастает проницаемость и уменьшается селективность. [15]
Страницы: 1