Замещение - молекула
Cтраница 3
При взаимодействии Rh ( HCOO) 20 5 H2O с аммиаком, хлористым аммонием, пиридином, соляно-кислым гуанидином и йодистым калием образуются соединения сложного состава. В этих реакциях не происходит замещения молекул формиата. Все соединения отличаются большой устойчивостью на воздухе. При нагревании с водным раствором аммиака разлагаются. [31]
Образец из Лакола представляет собой псевдоморфозу кварца по бериллу со следами берилла на некоторых гранях кристалла. Повидимому, здесь имеет место замещение молекулы берилла молекулой кварца, так как в псевдо морфозах сохранилась первичная трещиноватость берилла по базису. Другой образец содержит выделение кварца в ядре большого кристалла берилла. [32]
Выше рассмотренные способы модификации ингредиентов в бинарных и сложных расплавах с получением простых эвтектических смесей, твердых растворов замещения, молекулярных комплексов и новых химических соединений [22, 23,34, 237] являются наиболее перспективными и с экологической точки зрения, поскольку при температуре, соответствующей эвтектической точке плавления, смеси пылящих порошкообразных ингредиентов могут образовывать прочные и легкоплавкие гранулы. В эвтектических смесях и твердых растворах замещения молекулы сохраняют индивидуальность, тогда как в молекулярных комплексах имеет место перераспределение электронной плотности [238] и избыточных зарядов. [33]
Процесс удаления лакокрасочных покрытий под действием органических растворителей можно рассматривать следующим образом: растворители в результате диффузионных процессов проникают в покрытие, при этом на скорость диффузии оказывают влияние многочисленные факторы, связанные со свойствами растворителей, пленкообразователей и их термодинамическим сродством. В результате проникновения растворителей к поверхности металла и замещения молекул полимера адсорбированного на подложке молекулами растворителя происходит нарушение адгезионной связи и отслаивание покрытий. Для лакокрасочных покрытий на основе термопластичных полимеров этот процесс заканчивается растворением пленки; покрытия на основе термореактивных полимеров набухают и отслаиваются от подложки. Адгезионная прочность покрытий зависит от типа подложки и степени подготовки поверхности. [34]
Статистическое распределение происходит далеко не всегда, в большинстве случаев наблюдается отклонение от него. Это связано с вторичными реакциями возбужденных в результате замещения молекул. [35]
Большинство широко используемых растворителей обладает до-норными свойствами, поэтому при реакциях комплексообразования в растворах происходит конкуренция между лигандами и молекулами растворителя. Такие реакции в растворах можно рассматривать как реакции замещения молекул растворителя, координированных ионом или молекулой, конкурирующими лигандами L или Х -, которые либо нейтральны, либо заряжены. [36]
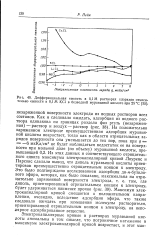 |
Дифференциальная емкость в 0 1М растворах хлоридов относительно емкости в 0 1 М КС1 в безводной муравьиной кислоте при 25 С. [37] |
Из этих данных и соответствующего отрицательного сдвига максимума электрокапиллярной кривой Лоуренс и Парсонс сделали вывод, что диполь муравьиной кислоты ориентирован преимущественно отрицательным концом к электроду. Максимум электрокапиллярной кривой смещается в положительном направлении, очевидно, вследствие адсорбции эфира, что также следовало ожидать при замещении молекулы растворителя, ориентированной отрицательным концом к электроду, на неполярное адсорбированное вещество. [38]
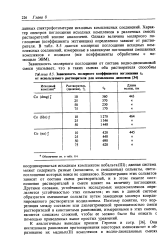 |
Зависимость молярного коэффициента поглощения ЕО от используемого растворителя для комплексов диоксима. [39] |
Концентрации этих сольватов зависят от состава смеси растворителей, и в этом смысле соотношение растворителей в смеси влияет на величину поглощения. Другими словами, устойчивость исследуемых иодокомплексов определяется устойчивостью этих сольватов; из них в данной системе образуются смешанные сольваты путем замещения молекул координированного растворителя иодид-ионом. Поэтому понятно, что корреляция между составом или диэлектрической проницаемостью смеси растворителей и константами равновесия, измеренными в этих смесях, является слишком сложной, чтобы ее можно было бы описать с помощью приведенных выше простых уравнений. [40]
Было показано, что у элементов подгруппы щелочноземельных металлов сумма изменений энтальпии при гидратации ионов галогенов и металла 2Я, настолько меньше Ем, что замещение молекул гидратной воды на ионы галогена кажется весьма маловероятным. Это мнение хорошо согласуется с экспериментом. Таким образом, вытеснение ионами хлора, брома и йода воды из гидратной оболочки катиона ртути должно неизменно сопровождаться уменьшением энтальпии. Последующая гидратация молекулы может только усилить этот эффект. [41]
Во втором условии, предусматривающем отсутствие твердого раствора в твердой фазе, должны быть отмечены следующие пункты. Склонность к образованию твердых растворов наиболее вероятна, если растворенные молекулы имеют примерно ту же величину и форму, что и молекулы основного компонента ( растворителя), что позволяет некоторым из этих последних замещаться молекулами растворенного вещества без плавления кристалла. Это замещение молекул основного компонента в кристаллической решетке подходящими молекулами растворенного вещества без плавления кристалла становится значительно более благоприятным, когда кристаллическая форма основного компонента получается ниже точки плавления как результат перехода с поглощением энергии, сравнимой с энергией, необходимой для плавления. Таким образом, этот переход соответствует до некоторой степени процессу, в котором кристалл почти расплавился. В этом случае кристалл, который имеет малую величину теплоты плавления, в точке плавления не очень отличается от жидкого состояния и обладает большой подвижностью структуры, что способствует значительному расширению возможности для молекул большей величины и разной формы, находящихся в растворе, войти в кристаллическую решетку без ее действительного плавления. Таким образом, образование твердого раствора можно предполагать в любой системе, где основной компонент имеет небольшую теплоту плавления. В результате обширных исследований, проведенных по исследовательной проблеме 6 АНИ, выяснилось, что низкомолекулярные углеводороды и их производные, которые чаще всего остаются в качестве загрязнений в данном веществе, после того как оно было подвергнуто многократному разделению, редко образуют твердые растворы. Исключение составляют лишь вышеупоминавшиеся случаи, когда основной компонент имеет малую теплоту плавления. [42]
В приведенных четырех системах молекулы компонентов, образующих отдельные системы, различаются наличием дополнительного шестичленного кольца. Твердые растворы никогда не образуются в первой из этих систем, так как очень велика относительная разница в размерах молекул бензола и нафталина. Зато в остальных системах происходит замещение молекул, отличающихся значительным объемом. [43]
Гримм оставляет открытым вопрос, входит ли в кристалл второй компонент в виде одной молекулы или в виде нескольких связанных между собою молекул. Однако он приводит схему, в которой показывает, каким образом могут быть компенсированы разные заряды ионов BaSO4 и КМпО4, даже если они входят в виде одной молекулы, для того чтобы создалось одинаковое расстояние между ионами. Но никаких доказательств в пользу возможности замещения молекулы за молекулу без изменения кристаллической решетки Гримм привести не может. [44]
Степень и скорость замещения практически не зависит от степени покрытия адсорбента полистиролом, а также от времени, в течение которого выдерживали раствор полистирола и адсорбент. Известно, что в зависимости от этих параметров могут происходить изменения конформации адсорбированных молекул. Очевидно, в исследованном случае при замещении молекул одного полимера молекулами другого никаких изменений в конформации цепей на поверхности адсорбента не происходит. [45]
Страницы: 1 2 3 4