Предсказание - скорость - реакция
Cтраница 2
Установление закона скорости необходимо по трем причинам. Первой причиной является возможность предсказания скорости реакции при данном составе смеси и экспериментальном значении константы скорости. Вторая причина - это то, что рассмотрение закона скорости предполагает установление механизма реакции и Приемлемый механизм должен соответствовать наблюдаемому закону скорости. Третья причина связана с классификацией реакций по различным порядкам. Порядок реакции - это степень, в которой концентрация компонента входит в уравнение скорости, а общий порядок - это сумма показателей степеней всех концентраций. Это означает, что реакция, подчиняющаяся закону скорости, выражаемому уравнением 26.2.2), является реакцией первого порядка по веществу А, первого порядка по В, с общим вторым порядком. Реакция с законом скорости, выраженным уравнением (26.2.3), также является реакцией первого порядка по А, но второго порядка по В и общего третьего порядка. Реакция не обяза-тельно имеет целые порядки; закон скорости, представленный уравнением (26.2.4), соответствует половинному порядку реакции по А и общему порядку, равному трем с половиной. [16]
Установление закона скорости необходимо по трем причинам. Первой причиной является возможность предсказания скорости реакции при данном составе смеси и экспериментальном значении константы скорости. Вторая причина - это то, что рассмотрение закона скорости предполагает установление механизма реакции и Приемлемый механизм должен соответствовать наблюдаемому закону скорости. Третья причина связана с классификацией реакций по различным порядкам. Порядок реакции - это степень, в которой концентрация компонента входит в уравнение скорости, а общий порядок - это сумма показателей степеней всех концентраций. Это означает, что реакция, подчиняющаяся закону скорости, выражаемому уравнением 26.2.2), является реакцией первого порядка по веществу А, первого порядка по В, с общим вторым порядком. Реакция с законом скорости, выраженным уравнением (26.2.3), также является реакцией первого порядка по А, но второго порядка по В и общего третьего порядка. Реакция не обязательно имеет целые порядки; закон скорости, представленный уравнением (26.2.4), соответствует половинному порядку реакции по А и общему порядку, равному трем с половиной. [17]
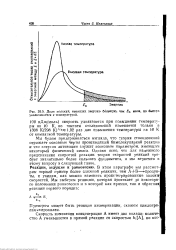 |
Доля молекул, имеющих энергию большую, чем., мала, но быстро увеличивается с температурой. [18] |
Мы будем придерживаться взгляда, что теория столкновений отражает основные черты происходящей бимолекулярной реакции и что энергия активации служит полезным параметром, имеющим некоторый физический смысл. Однако ясно, что для надежного предсказания скоростей реакции теория скоростей реакций требует значительно более сильного фундамента, и мы вернемся к этому вопросу в следующей главе. Реакции, ведущие к равновесию. В этом параграфе мы рассмот - j рим первый пример более сложной реакции, чем А В-э-лродук - ты, и увидим, как можно изменить проинтегрированные законы. Мы выберем реакцию, которая протекает до некоторо-1 го положения равновесия и в которой как Прямая, так я обратная. [19]
Мы будем придерживаться взгляда, что теория столкновений отражает основные черты происходящей бимолекулярной реакции н что энергия активации служит полезным параметром, имеющим некоторый физический смысл. Однако ясно, что для надежного предсказания скоростей реакции теория скоростей реакций требует значительно более сильного фундамента, н мы вернемся к этому вопросу в следующей главе. [20]
Аналогично нельзя ожидать, что значения констант Гаммета о можно использовать для корреляции данных по скоростям, полученным для реакций электрофильного замещения, когда электронодонорные заместители ( - R) находятся в пара-положении. Было предложено несколько соотношений [ И, 76 ] для таких электрофильных реакций, использующих значения а, которые давали удовлетворительные предсказания скоростей реакций в этих случаях. [21]
Воронка с наиболее узкой трубкой будет играть роль горлышка бутылки, и в случае если диаметр ее трубки значительно меньше, чем у остальных воронок, она одна будет определять скорость протекания песка. В целом многостадийная химическая реакция включает медленную стадию, определяющую скорость ( аналогичную воронке с узкой трубкой), и другие, относительно быстрые стадии, которые могут осуществляться как раньше, так и позднее медленной тадии. Предсказание скорости реакции, протекающей по стадийному механизму, должно включать в качестве центральной проблемы выяснение того, какая из стадий определяет скорость, и анализ факторов, определяющих скорость этой стадии. [23]
Воронка с наиболее узкой трубкой будет играть роль горлышка бутылки, и в случае если диаметр ее трубки значительно меньше, чем у остальных воронок, она одна будет определять скорость протекания песка. В целом многостадийная химическая реакция включает медленную стадию, определяющую скорость ( аналогичную воронке с узкой трубкой), и другие, относительно быстрые стадии, которые могут осуществляться как раньше, так и позднее медленной стадии. Предсказание скорости реакции, протекающей по стадийному механизму, должно включать в качестве центральной проблемы выяснение того, какая из стадий определяет скорость, и анализ факторов, определяющих скорость этой стадии. [25]
Это определение свободной энергии в качестве истинной термодинамической функции зависит только от природы двух фиксированных состояний. Такими двумя фиксированными состояниями в этом случае являются исходное и переходное состояния реакции. Поэтому, если имеются достаточные сведения о строении исходных веществ и переходном состоянии, то в принципе возможно и предсказание скорости реакции. [26]
В первом разделе настоящей главы был уже указан путь, по которому устанавливается связь скорости реакции с молекулярными характеристиками исходных веществ и переходного ( активированного) комплекса. Метод активированного комплекса позволяет, в принципе, рассчитать константу скорости химической реакции. Однако практически при решении данной задачи возникают значительные трудности, которые препятствуют расчету поверхностей потенциальной энергии с точностью, достаточной для предсказания скорости реакции. [27]
Страницы: 1 2

