Электрофильное замещение - водород
Cтраница 3
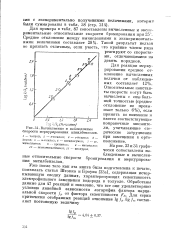 |
Вычисленные и наблюденные скорости меркурирования алкилбензолов. [31] |
Уже после того как эта книга была подготовлена к печати, появилась статья Штокка и Броуна [ ЗЗа ], содержащая исчерпывающую сводку данных, характеризующих селективность электрофильного замещения водорода в толуоле. [32]
Важный вопрос о влиянии реагента на реакционную способность вещества при химических реакциях и на механизм последних, пожалуй, наиболее подробно разобран на примере изменения правил ориентации при электрофильном замещении водорода в ароматических соединениях, и ему посвящена вторая глава. [33]
В отличие от бензола, у которого молекула не имеет дипольного момента, атом азота пиридинового кольца как более электроотрицательный, чем углерод, образует самую большую электронную плотность возле себя и меньшую возле атомов углерода, что проявляется в сравнительно большом дипольном моменте в молекуле пиридина, равном 2.2 D, в наличии основных свойств, в затруднении реакций электрофильного замещения водорода, в облегчении нуклеофильного замещения. [34]
Установлено, что кислотно-катализируемое хлорирование ароматических эфиров алкилгипохлоритами при 20 - 25 С приводит к образованию моно - и дихлорзамещен-ных в ароматическом кольце производных. Электрофильное замещение водорода преимущественно осуществляется при атоме углерода в пара - положении к алкок-сильной группе. [35]
Гидроксильная группа относится к числу наиболее сильных орто-пара-ориентантов. Реакции электрофильного замещения водорода в бензольном ядре для фенолов проходят значительно легче и в более мягких условиях, чем для бензола. [36]
Изменение химической природы реагента и свойств среды дает также возможность выявить разные стороны взаимного влияния атомов в молекуле одного и того же вещества. Так, при реакциях электрофильного замещения водорода в ароматических соединениях обычно превалирует эффект сопряжения, а при реакциях протофильного замещения водорода на первый план выступает эффект индуктивного сдвига электронов. Если заменить электрофильный реагент на нуклеофильный, то происходит обращение правил ориентации замещения водорода в ароматическом кольце; мало того, они изменяются даже в том случае, когда резко повышается химическая активность pea гентов данного типа. [37]
Изучение изотопных эффектов в реакциях ароматического замещения [56], показало, что в реакциях нитрования и бромирования с участием электрофила Вг отрыв протона не происходит на стадии, лимитирующей скорость, а при сульфировании, азосочетании, водородном обмене, галогенировании в разных условиях разрыв связи С - Н может, по крайней мере частично, определять скорость процесса. Отсутствие изотопного эффекта в некоторых реакциях электрофильного замещения водорода подтверждает наличие двух или более элементарных стадий, так как исключает возможность одностадийного синхронного механизма, при котором атом водорода неизбежно отрывается на лимитирующей стадии. [38]
Ингольд [56] этерцфикацию спиртов рассматривает как 0-нитро-вание. Точнее, он считает, что происходит электрофильное замещение водорода гидроксила на нитрогруппу. [39]
Устойчивые аренониевые ионы привлекают пристальное внимание исследователей в связи с тем, что они являются аналогами промежуточных образований ряда важных реакций ароматических соединений. В первую очередь это относится к реакциям электрофильного замещения водорода в ароматическом ядре [5-11], а также к кислотно-катализируемым превращениям, связанным с изменением расположения заместителей в ароматической молекуле ( реакции изомеризации [12, 13]) и с межмолекулярным переносом заместителей. [40]
Несомненно, что эти реакции обычно протекают аналогично другим электрофильным замещениям водородов ароматического ядра. Предлагаемые универсальные схемы не выдерживают критики, так как не отвечают многим экспериментальным фактам. [41]
Наиболее часто этот способ используется для того, чтобы исключить возможность протекания электрофильного замещения водорода в соответствующей гидроксильной группы. Однако в случае вторичных спиртов переход к тритильным группы существенно облегчает отрыв гидрид-иона от сс - СН-фрагмента под действием таких специфических катализаторов, как тритил-катион, в результате чего может достаточно легко происходить дис-пропорционирование с образованием кетонного фрагмента и трифенилме-тана. [42]
Методы получения полифторароматических соединений отличаются от методов получения ароматических соединений. Если в химии ароматических углеводородов основным методом введения функциональных групп являются реакции электрофильного замещения водорода, то в химии полифторароматических соединений важнейшими являются реакции нуклеофильного замещения фтора. Кроме того, наличие полифторированного ароматического кольца оказывает весьма специфическое влияние и на превращения связанных с ним заместителей. [43]
Такие процессы особенно интенсивно изучались на примере арилсиланов и арилстаннанов. Существенное отличие состоит в том, что скорость таких процессов значительно выше, чем скорость электрофильного замещения водорода. Гетероциклические аналоги таких эле-ментоорганических производных также вступают в реакции мясо-замещения, и в случае электроноизбыточных систем, вероятно, сохраняется тот же механизм. [44]
Для реакции предлагается механизм злектрофильного замещения с образованием промежуточного протони ров энного комплекса. Этот механизм подтверждается линейной зависимостью логарифмов констант скорости протодесилилирования от логарифмов относительных скоростей известных реакций электрофильного замещения водорода в соответствующих положениях ксилолов. [45]
Страницы: 1 2 3 4