Запас - энергия - электрон
Cтраница 1
 |
Возможные переходы электрона. [1] |
Запас энергии электрона определяет уровень энергии ( энергетический уровень), которой обладает электрон. [2]
При этом запас энергии электрона уменьшается, а значит, и энергия его излучения тоже, что должно привести к непрерывному изменению длин волн, испускаемых атомами лучей. Казалось, атом должен излучать волны всех длин от минимальной Лмин, отвечающей максимуму энергии электрона, до максимальной макс, отвечающей минимальной энергии электрона. [3]
По мере удаления от ядра запас энергии электронов увеличивается. Связь электронов с положительно заряженным ядром в этом же направлении ослабевает. [4]
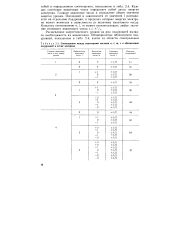 |
Соотношения между квантовыми числами п, I, m, s и обозначения подуровней в атоме водорода. [5] |
Каждое сочетание квантовых чисел определяет собой запас энергии электрона. Главное квантовое число п определяет общее значение энергии уровня. Последний в зависимости от значения / распадается на отдельные Подуровни, в пределах которых энергия электрона может меняться в зависимости от величины квантового числа. [6]
Число подуровней в каждом энергетическом уровне равно его главному квантовому числу. Главное и орбитальное квантовые числа характеризуют запас энергии электрона. [7]
Спектры атомов оказались более сложными, чем это вытекает из теории Бора. В спектрах наблюдаются такие линии, частоты которых показывают, что запасы энергии электронов, расположенных на одном энергетическом уровне, несколько различаются между собой. На основании этого электроны каждого слоя объединены в подгруппы, или подуровни. [8]
 |
Схема установки для определения ионизационных потенциалов. [9] |
Сила тока, фиксируемая гальванометром, растет. В процессе своего перемещения от катода к аноду электроны встречают на пути пар, состоящий из атомов исследуемого элемента. Пока запас энергии электронов меньше кванта, необходимого для возбуждения атома элемента, эти столкновения носят характер упругих столкновений и не изменяют запаса энергии атома. Начиная с этого момента дальнейшее повышение напряжения между электродами приводит к быстрому нарастанию силы тока. [10]
Электроны в атомах располагаются слоями ( электронные слои), находящимися на определенном расстоянии от ядра и друг от друга. Электронные слои ина е называются Энергетическими уровнями. Они характеризуют запас энергии электронов. [11]
 |
Электронное облако водо - 3РенИЯ квантовой механики. Электрон рода с неравномерной плотно - атома водорода образует электронное об-стью лако формы шара. Как видно из рисунка. [12] |
Иногда их обозначают буквами / С, L, M, N, О, Р, Q. Целое число п, обозначающее номер уровня, называется главным квантовым числом. Оно характеризует запас энергии электронов, занимающих данный энергетический уровень. [13]
 |
Возможные переходы электрона ( в атоме водорода, определяющие полосы в его спектре излучения. [14] |
Следовательно, атом может поглощать не любые, а вполне определенные порции энергии. При этом электроны удаляются от ядра, перескакивая на более дальние стационарные орбиты. При обратном перескоке электронов атом возвращается в нормальное состояние, испуская точно такие же кванты энергии. Энергия электрона является его основной характеристикой, определяющей орбиту электрона. Запас энергии электрона определяет уровень энергии ( энергетический уровень), которой обладает электрон. Чем дальше друг от друга расположены энергетические уровни, между которыми происходит переход электрона, тем больше частота v квантов энергии ( рис. 3), поглощаемых или испускаемых атомами. [15]
Страницы: 1 2