Наиболее характерная валентность
Cтраница 1
Наиболее характерные валентности выделены жирным шрифтом, а наименее характерные или малоизученные даны в скобках. Как видно из приведенного сопоставления, первоначально ( от Th до U) имеет место возрастание наиболее характерной валентности, а затем ( от U до Cm) - ее снижение. [1]
Наиболее характерные валентности выделены жирным шрифтом, а не характерные или малоизученные даны в скобках. Как видно из приведенного сопоставления, от Th до U наиболее характерные валентности возрастают, а затем снижаются. [2]
Наиболее характерные валентности выделены жирным шрифтом, а нехарактерные или малоизученные даны в скобках. Как видно из приведенного сопоставления, наиболее характерные валентности, возрастают, а затем снижаются. [3]
Наиболее характерные валентности выделены жирным шрифтом, а наименее характерные или малоизученные даны в скобках. Как видно из приведенного сопоставления, первоначально ( от Th до11) имеет место возрастание наиболее характерной валентности, а затем - ее снижение. [4]
Наиболее характерными валентностями всех других атомов являются валентности в таких соединениях, в которых структура наружной электронной оболочки атома приобретает вид структуры наружных оболочек атомов инертных газов. Так, например, наружная оболочка атома серы 3s2p для образования структуры типа аргона должна пополниться двумя / 7-электронами, а для образования структуры типа неона надо вырвать шесть электронов из этой оболочки. [5]
Какие наиболее характерные валентности имеют элементы подгруппы азота. [6]
Причина различия наиболее характерной валентности меди, серебра и золота не может быть объяснена на основании качественных соображений относительно особенностей строения их атомов. [7]
Валентность - приводятся наиболее характерные валентности элементов ( о валентности по кислороду и водороду см. стр. [8]
Валентность - приводятся наиболее характерные валентности элементов ( о валентности по кислороду см. стр. [9]
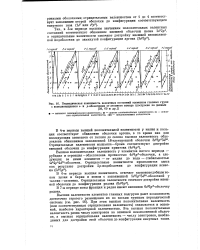 |
Периодическая зависимость валентных состояний элементов главных групп с заполняющимися s - и р-оболочками от атомного номера ( построено по данным. [10] |
При этом высшая положительная валентность или соответствующая отрицательная валентность) оказывается и основной, наиболее характерной валентностью. Эта высшая положительная валентность равна числу электронов во внешней незаполненной оболочке, а высшая отрицательная валентность - числу электронов, необходимых для достройки этой оболочки до конфигурации инертных газов. [11]
Многие лантаноиды и актиноиды обладают рядом валентных состояний, и, хотя иногда трудно указать наиболее характерную валентность, кривые имеют периодический характер с двумя максимумами и двумя минимумами. Следовательно, периодичность изменения валентных состояний с возрастанием атомного номера проявляется и при заполнении наиболее глубоких / - оболочек, хотя и в менее отчетливой форме, чем при заполнении d - оболочек или самых внешних s - и р-оболочек. Чем глубже заполняющаяся оболочка, тем естественно и менее ярко выражена периодичность валентных состояний. [12]
 |
Температуры плавления металлов больших периодов. [13] |
Вопрос о заряде металлических ионов в кристаллических решетках является весьма сложным и естественно при оценке этого заряда ориентироваться на наиболее характерные валентности этих металлов в химических соединениях. Они выбраны с учетом высшей или характерной валентности соответствующих металлов в неорганических соединениях с учетом данных о числе свободных электронов по постоянной Холла для металлов I и II групп. [14]
Инертные газы расположены в конце периодов системы Менделеева, и структура их наружных электронных оболочек, содержащих два электрона в первом периоде ( гелий Is2) и по восемь электронов во всех остальных периодах ( от неона - 2s2p6 до радона - 6s2p6), является наиболее устойчивой. Наиболее характерными валентностями всех других атомов являются валентности в таких соединениях, в которых структура наружной электронной оболочки атома приобретает вид структуры наружных оболочек атомов инертных газов. Так, например, в наружную оболочку атома серы 3s2p4 для образования структуры типа аргона должно прибавиться два / 7-электрона, а для образования структуры типа неона надо оторвать шесть электронов из этой оболочки. По мере перехода в рамках первых периодов системы Менделеева слева направо возрастает число электронов в наружных оболочках атомов. [15]
Страницы: 1 2