Электростатическая валентность
Cтраница 1
Теория электростатической валентности была создана за несколько лет ( Коссель, 1916 г.) до описываемых работ по кристаллохимии ( 1920 г.) и к этому времени достаточно прочно вошла в химию. [1]
Теория электростатической валентности была создана за несколько лет ( Коесель, 1916 г.) до описываемых работ по кристаллохимии ( 1920 г.) и к этому времени достаточно прочно вошла в химию. Кроме того, атом натрия потерял один электрон и, следовательно, удерживает остальные прочнее, чем атом хлора, получивший лишний электрон. [2]
Правило электростатической валентности приблизительно удовлетворяется для ионов гидроксила ( 1 17) и для большинства ионов кислорода, но не для кислорода в подчиненных позициях. [3]
Применение правила электростатической валентности Паулиига, в соответствии с которым валентность алюминия - f - 3 распределяется между шестью кислородно-алюминиевыми связями, приводит к тому, что водороды в молекуле координированной воды оказываются подвижными и что образуется кислота типа Брен-стеда. Подобная же структура, содержащая магний с координационным числом 4 в магниевосиликатных катализаторах или цирконий с координационным числом 6 в силикатных катализаторах, тоже будет представлять собой относительно сильную кислоту типа Бренстеда. [4]
В соответствии с правилом электростатической валентности наиболее устойчивыми структурами кристаллов и молекул являются такие, в которых сумма прочностей связей каждого аниона точно равна его отрицательному заряду. [5]
 |
Структура дистена. [6] |
Таким образом, правило электростатической валентности выдерживается, поскольку каждый ион кислорода одну валентность расходует на связь с ионом кремния, а на связь с каждым ионом магния остается 7з валентности. [7]
Таким образом, правило электростатической валентности выдерживается, поскольку каждый ион кислорода одну валентность расходует на связь с ионом кремния, а на связь с каждым ионом магния остается / з валентности. [8]
 |
Возможные сочетания двух тетраэдров и. [9] |
Второе правило, носящее название правила электростатической валентности, гласит, что в устойчивой ионной структуре валентность каждого аниона точно или приблизительно равна сумме валентных усилий этого аниона с соседними с ним катионами. [10]
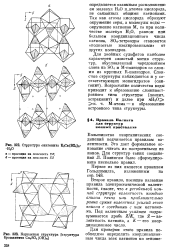 |
Структура сингенита К2Са ( 80ч 1 - Н20.| Каркасная структура [ структура брошантита Сщ804 ( ОН в ]. [11] |
Второе правило, носящее название правила электростатической валентности, гласит, что в устойчивой ионной структуре валентность каждого аниона точно или приблизительно равна сумме валентных усилий этого аниона с соседними с ним катионами. Под валентным усилием подразумевается дробь Z / K, где Z - валентность катиона, а А - его координационное число. [12]
Следовательно, для структуры перовскита правило электростатической валентности точно выполняется. [13]
Баур [93], основываясь на правиле электростатической валентности Полинга, показал, что для 5Ю4 - тетраэдров силикатов существует простое соотношение между длиной связи и усилием связи, получаемым данным анионом от окружающих его катионов. [14]
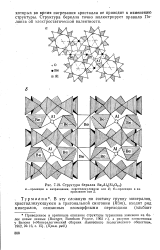 |
Структура берилла Ве3А12 [ 5. бО18 ]. [15] |
Страницы: 1 2 3