Ненасыщенная валентность
Cтраница 3
Исходные продукты превращаются в конечные только с участием промежуточных соединений - осколков молекул с ненасыщенными валентностями. [31]
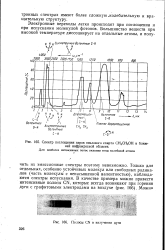 |
Спектр поглощения паров этилового спирта СН3СН2ОН в ближней инфракрасной области.| Полосы CN в излучении дуги. [32] |
Только для отдельных, особенно устойчивых молекул или свободных радикалов ( часть молекулы с ненасыщенной валентностью), наблюдаются спектры испускания. [33]
Исходные продукты превращаются в конечные только с участием промежуточных соединений - осколков молекул с ненасыщенными валентностями. [34]
Кристалл в целом представляет собой, таким образом, некую макроскопическую молекулу, обладающую ненасыщенными валентностями; его можно рассматривать как своего рода полирадикал. Нам хорошо известна роль, которую играют свободные радикалы в кинетике гомогенных химических реакций. В случае катализа свободные валентности вносятся самим катализатором. Введение в игру этих свободных валентностей стимулирует реакцию. Мы приходим к представлению о кристаллическом катализаторе как об особого рода полирадикале. Этим стирается исторически сложившееся мнение о существовании принципиального различия между гетерогенным катализом и кинетикой гомогенных химических реакций. [35]
Свободный радикал является молекулой, содержащей по крайней море один песпаренный электрон и поэтому имеющий ненасыщенную валентность. По способу получения и свойствам свободные радикалы напоминают атомы. Они всегда неустойчивы и быстро соединяются друг с другом или реагируют со стабильными молекулами. [36]
С этой точки зрения зарождение цепи всегда заключается в реакции образования атома или радикала с ненасыщенной валентностью, как. Это может гфрнлхшшть в результате течмш с кой диссоциации какой-ниб дь легко распадающейся молекулы ( напримзр, J2ZiJ - rJ), при столкновении двух молекул, обладающих повышенной энергией, при ударе молекулы о стенку сосуда или в особенности при химическом взаимодействии ее с атсмами или ионами ( поверхности стенки или находящимися в объеме сосуда), способными вызвать при этом образование радикала. [37]
Лэнгмюр в своей теории учитывал только энергетически неоднородную поверхность, считая, что поверхностные частицы с ненасыщенными валентностями создают элементарные участки с более высокими потенциалами. Однако такие молекулы не занимают особого положения с точки зрения геометрии и структуры поверхности. Теория Лэнгмюра сводится к трем постулатам: 1) поверхность состоит из ограниченного числа идентичных участков, 2) нет взаимодействия между адсорбированными молекулами и 3) образование хемосорбированного монослоя. Такие условные ограничения значительно лимитируют понимание сути гетерогенного катализа. Хорошо известно, что чем более неоднородна поверхность, тем интенсивнее и с тем большим термическим эффектом протекают адсорбция и хемосорбция, неразрывно связанные с гетерогенным катализом. [38]
Лэнгмюр дает кинетическое обоснование процессу адсорбции, исходя из представления о том, что адсорбция обусловливается существованием ненасыщенных валентностей на поверхности адсорбента. Молекулы адсорбируемого газа, совершая тепловое движение, попадают в сферу притяжения этих участков и адсорбируются. Происходит их уплотнение, конденсация на поверхности адсорбента. Но одновременно некоторые из уже адсорбированных молекул вследствие того же теплового движения, обладая достаточной кинетической энергией, отрываются от поверхности, испаряясь с нее. В конце концов устанавливается статистическое равновесие-за единицу времени количество испаряющихся молекул равно количеству конденсирующихся. Это равновесие наступает тогда, когда скорость конденсации, рассчитанная на 1 см2 поверхности, становится равной скорости испарения. [39]
По мнению Н. Н. Семенова, цепные реакции протекают обычно через образование и взаимодействие радикалов или свободных атомов с ненасыщенной валентностью. Этот путь взаимодействия является преимущественным по сравнению с взаимодействием валентно насыщенных молекул, потому что свободная валентность придает радикалу ( или атому) весьма высокую реакционную спо - собность, что дает ему возможность легко вовлекать во взаимодействие и валентно насыщенные молекулы, как, например, в реакциях ( б), ( в) и ( д) рассмотренного процесса. [40]
По мнению Н. Н. Семенова, цепные реакции протекают обычно через образование и взаимодействие радикалов или свободных атомов с ненасыщенной валентностью. Этот путь взаимодействия является преимущественным по сравнению с взаимодействием валентно насыщенных молекул, потому что свободная валентность придает радикалу ( или атому) весьма высокую реакционную спо-ссбьость, что дает ему возможнссть легко вовлекать во взаимодействие и валентно насыщенные молекулы, как, например, в реакциях ( б), ( в) и ( д) рассмотренного процесса. [41]
По мнению Н. Н. Семенова, все цепные реакции протекают через образование и взаимодействие радикалов или свободных атомов с ненасыщенной валентностью. Этот путь взаимодействия является преимущественным по сравнению с взаимодействием валентно-насыщенных молекул, потому что свободная валентность придает радикалу ( или атому) весьма высокую реакционную способность, дающую ему возможность легко вовлекать во взаимодействие и валентно-насыщенные молекулы, как, например, в реакциях ( б), ( в) и ( д) рассмотренного процесса. [42]
По мнению Н. Н. Семенова, цепные реакции протекают обычно через образование и взаимодействие радикалов или свободных атомов с ненасыщенной валентностью. Этот путь взаимодействия является преимущественным по сравнению с взаимодействием валентно насыщенных молекул, потому что свободная валентность придает радикалу ( или атому) весьма высокую реакционную способность, что дает ему возможность легко вовлекать во взаимодействие и валентно насыщенные молекулы, как, например, в реакциях ( б), ( в) и ( д) рассмотренного процесса. [43]
По мнению Н. Н. Семенова, цепные реакции протекают обычно через образование и взаимодействие радикалов или свободных атомов с ненасыщенной валентностью. Этот путь взаимодействия является преимущественным по сравнению с взаимодействием валентно насыщенных - молекул, потому что свободная валентность придает радикалу ( или атому) весьма высокую реакционную способность, что дает ему возможность легко вовлекать во взаимодействие и валентно насыщенные молекулы, как, например, в реакциях ( б), ( в) и ( д) рассмотренного процесса. [44]
Наличие в молекулах некоторых веществ определенных групп атомов ( С, Н, О, N) с ненасыщенными валентностями ( радикалы) может приводить к появлению полос поглощения, лежащих в видимой области спектра. Наличие полос поглощения придает веществу окраску, обусловленную выбыванием ( или более или менее сильным ослаблением) излучения с длинами волн, соответствующими этим полосам. Такие группы называют цветоносителями или хромофорными группами. [45]
Страницы: 1 2 3 4