Принцип - термодинамика
Cтраница 2
Согласно принципам термодинамики, дисперсные системы не могут быть получены самопроизвольно. Для этого необходимо совершить определенные действия, связанные с затратой энергии. [16]
 |
Изменение свободной энергии в ходе реакции А В - - Q D. - ДО - свободная энергия реакции. [17] |
Продолжая применять принципы термодинамики к переходному состоянию, вместо величины ДО подставляем ее значение из уравнения ( 22) ( стр. [18]
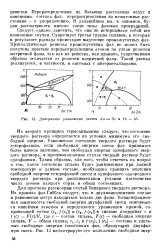 |
Диаграммы равновесия систем Аи - Ш и Fe - Al. [19] |
Из второго принципа термодинамики следует, что состояние твердого раствора определяется из условия минимума его свободной энергии. Равновесное состояние твердого раствора будет гетерофазным, если свободная энергия смеси фаз принимает более низкое значение, чем свободная энергия однофазного твердого раствора, в противоположном случае твердый раствор будет однофазным. Таким образом, для того, чтобы ответить на вопрос о том, какое состояние сплава будет равновесным при данной температуре и данном составе, необходимо сравнить значения свободной энергии гетерофазной смеси и однофазного однородного твердого раствора при дополнительном условии постоянства числа атомов каждого сорта в обоих состояниях. [20]
Возможность приложения принципов термодинамики к жизненным явлениям тесно связана с вопросом о природе сил, действующих в организме. Исследование проблемы о подчинении процессов в живых тканях и клетках основным законам физики и химии, помимо научного и практического интереса для естествознания и обыденной жизни, имеет колоссальное философское значение. [21]
Изложенные два принципа термодинамики необратимых процессов, выраженные в виде системы линейных уравнений, имеют ограничение в виде принципа Кюри, который заключается в следующем. [22]
Согласно второму принципу термодинамики, в системах, обладающих избытком свободной энергии, могут самопроизвольно протекать процессы, понижающие запас энергии. Уменьшение же а может происходить за счет притяжения к поверхности из дисперсионной среды молекул или атомов. [23]
Согласно второму принципу термодинамики энтропия энергетически замкнутой молекулярной системы с течением времени увеличивается, а свободная энергия уменьшается. [24]
Согласно второму принципу термодинамики передача тепла от низшего температурного уровня к высшему может происходить только при дополнительной затрате энергии извне. Так-как при обратном процессе энтропия участвующих в нем тел должна была бы уменьшиться, то для его проведения необходимо одновременно осуществить дополнительный процесс, сопровождающийся таким возрастанием энтропии, в результате которого энтропия всей системы остается без изменения или увеличивается. [25]
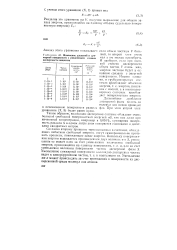 |
Изменение удельной и суммарной поверхности с увеличением степени дисперсности вещества. [26] |
Согласно второму принципу термодинамики в системах, обладающих избытком свободной энергии, могут самопроизвольно протекать процессы, понижающие запас энергии. Уменьшение же а может происходить за счет притяжения к поверхности из дисперсионной среды молекул или атомов. [27]
Согласно второму принципу термодинамики, природные процессы имеют направленность. [28]
Согласно второму принципу термодинамики, самопроизвольный процесс в изолированной системе происходит, если энтропия возрастает. Таким образом, в этой системе кристаллизация никогда не могла бы произойти, грубо говоря, потому, что некуда было бы отводить тепло. Однако в реальных условиях плавящееся тело не является изолированным ( тепло можно отводить и. [29]
 |
Модели предельных состояний ССЕ.| Схема изменения толщины Н межфазного слоя при внешних воздействиях. [30] |
Страницы: 1 2 3 4