Природа - металл - электрод
Cтраница 1
 |
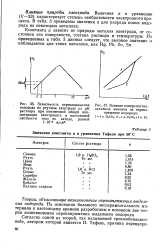
Зависимость хода анодных поляризационных кривых, снятых на Pt в 1 н. растворе H2SO4 при 20 С, от давления Н2 ( по Феттеру и Отто 164. [1] |
Природа металла электрода оказывает большое влияние на перенапряжение водорода. Уже в 1924 г. Бонгеффер 30 установил тесную связь между водородным перенапряжением и каталитической активностью металлов, а именно: перенапряжение будет тем меньше, чем больше каталитическая активность поверхности электрода в отношении реакций в газовой фазе. [2]
Константа а зависит от природы металла электрода, от состояния его поверхности, состава раствора и температуры. [4]
Она хорошо объясняет зависимость константы а от природы металла электрода его каталитическим действием, но не может объяснить других фактов. Все же эта теория может применяться в некоторых случаях. Третья стадия отражает роль адсорбции в перенапряжении. [5]
Константы а и К сильно зависят от природы металла электрода. [6]
Меняя форму, силу и продолжительность наложенного тока и другие условия работы электрода ( природу металла электрода, температуру, состав ванны), получаем феноменологическую таблицу кинетического поведения электрода, дающую возможность ответить на все возникающие вопросы. [7]
Гайсинским [10] была предложена гипотеза, объясняющая факт независимости критического потенциала осаждения радиоактивных элементов от природы металла электрода энергетической гетерогенностью металлической поверхности электрода. [8]
Сборник посвящен наиболее важным разделам электрохимии органических соединений: кинетике электродных процессов, электросинтезу, влиянию природы металла электрода на процессы адсорбции, электроокисления и электровосстановления органических веществ, полярографии. [9]
Уравнения (1.30) и ( 1.30 а) являются определением электрохимического равновесия, поэтому они не зависят от природы металла электрода. AG одинаково для любого металла. [10]
Однако, в литературе не известны соотношения, устанавливающие количественную связь между величинами Р и величинами, характеризую щими природу металла электрода. Между тем учитывая факт различных значений перенапряжения водорода и дейтерия, следует ожидать наличие определенной связи между величинами Р и природой металла. [11]
Здесь ki - константа скорости реакции Н - - Н - Н2; &2 - адсорбционная емкость электрода; п - величина ( обычно от 1 до 5), зависящая от природы металла электрода и степени насыщения его водородом. [12]
 |
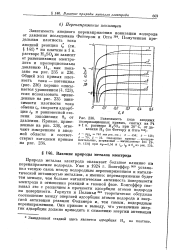
Зависимость логарифма плотности тока обмена от логарифма концентрации реагирующего вещества. [13] |
Величина yfej зависит от природы рассматриваемой окислительно-восстановительной системы и от растворителя. От природы металла электрода, согласно теории замедленного разряда, величина не зависит. [14]
Выходы растут с увеличением атомного номера катиона щелочного металла в электролите и уменьшаются в присутствии органического растворителя. Оптимальная плотность тока за-оисит от природы металла электрода. [15]
Страницы: 1 2