Природа - кристаллическая решетка
Cтраница 1
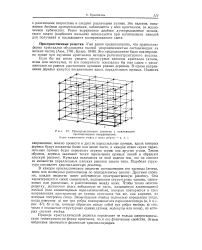 |
Пространственная решетка с наклонными. [1] |
Природа кристаллической решетки определяет не только макроскопическую геометрическую форму кристалла, но и его физические свойства. Этими вопросами занимается физическая кристаллография. [2]
Природа кристаллической решетки ( структуры) и расположение в ней атомов оказывают большое влияние на многие свойства металла, а также на коррозионную стойкость их. При коррозии кристаллическая решетка металла разрушается. Скорость этого процесса зависит от структуры металла, агрессшиюстн среды и многих других факторов. [3]
Благодаря самой природе кристаллической решетки ( которая у цеолитов всегда существует до начала процесса включения) включение молекул в пустоты имеет адсорбционный характер и меньше зависит от формы пустот кристаллической решетки. Однако знание размеров этих пустот позволяет подобрать соответствующие цеолиты при разделении углеводородов в зависимости от размеров их молекул. В настоящее время налажено производство цеолитов ( молекулярных сит) с поперечным сечением пустот от 4 до 11 А. Так, цеолиты, содержащие Na, служат для разделения молекулы сечением менее 4 А, а содержащие Са, разделяют молекулы сечением менее 5 А. [4]
В зависимости от строения атомов и природы кристаллических решеток валентная зона и зона проводимости могут перекрываться или не перекрываться. В случае, когда зоны не перекрываются, между ними имеется энергетический разрыв, который называется запрещенной зоной. Различие между металлами и полупроводниками определяется прежде всего энергетическим состоянием электронов проводимости. [5]
Причина общности как физических, так и химических свойств металлов лежит в общности строения их атомов и природы кристаллических решеток металлов. [6]
Причина общности как физических, так и химических свойств металлов лежит в общности строения их атомов и природы кристаллических решеток металлов. [7]
Причина общности как физических, так и химических свойств, металлов лежит в общности строения их атомов и природы кристаллических решеток металлов. [8]
 |
Схема роста кристаллов в застывающем расплаве. [9] |
Металлы в твердом состоянии имеют кристаллическое строение. Природа кристаллической решетки ( структура) и расположение в ней атомов влияют на ряд свойств металлов. [10]
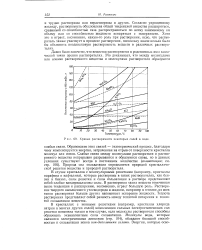 |
Кривые растворимости некоторых солей в воде. [11] |
Образование этих связей - экзотермический процесс, благодаря чему компенсируется энергия, затраченная на отрыв от поверхности кристалла молекул или ионов. Слабые связи между молекулами растворителя и растворенного вещества непрерывно разрываются и образуются снова, но в данных условиях существуют всегда в постоянном количестве ( сольватация; см. стр. Природа сил сольватации определяется природой кристаллической решетки вещества и природой растворителя. [12]
Хром может образовывать твердые растворы и металлические соединения. Кислород, азот и другие малорастворимые элементы при незначительном содержании их в хроме делают его хрупким при комнатной и повышенных температурах. Полагают, что малая пластичность хрома и сплавов на его основе определяется природой кристаллической решетки, чувствительной даже к весьма малому количеству примесей. Природа хрупкости хрома остается до настоящего времени мало изученной, и еще не решена полностью проблема получения пластичного хрома. [13]
Страницы: 1