Природа - щелочь
Cтраница 1
Природа щелочи в этом случае роли не играет, так как из данных рассчитывается лишь количество грамм-эквивалентов ее, участвующее в реакции нейтрализации. [1]
Природа щелочи мало влияет на величину перенапряжения водорода, с ростом концентрации щелочи перенапряжение снижается. [3]
Согласно приведенному механизму природа щелочи не должна влиять на кинетические параметры. [4]
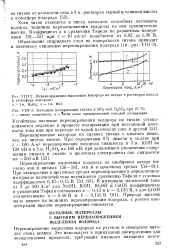
На процесс омыления влияют природа щелочей и вид исходной системы. В гуминовых препаратах из угля и акрило нитрила с КОН ( 40 %) нитрил ьная полоса остается ( при 2250 и 2255 см 1), а при омылении NaOH ( 40 %) она исчезает. В сополимерах из нитролигнина и акрилонитрила полоса поглощения нитрильной группы, наоборот, сохраняется при омылении едким натром ( рис. 3, б в), но исчезает при гидролизе КОН. [5]
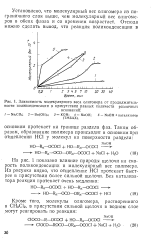 |
Зависимость молекулярного веса олигомера от продолжительности поликонденсации в присутствии равных количеств различных. [6] |
На рис. 1 показано влияние природы щелочи на скорость поликонденсации и молекулярный вес полимера. Из рисунка видно, что отщепление НС1 протекает быстрее в присутствии более сильной щелочи. [7]
Скорость превращения красящих оснований в бесцветные зависит и от природы щелочи. Аммиак вызывает очень быстрый переход в карбинольную форму. [8]
Изучение карбонизации растворов алюминатов с высоким содержанием щелочей с определением природы щелочи в гидрате, Отч. [9]
Напряжение разложения растворов щелочей и кислородных кислот практически не зависит от природы щелочи и кислоты. [10]
Механизм щелочного гидролиза рибонуклеиновых кислот имеет, несомненно, общее значение независимо от природы щелочи, примененной для гидролиза. Однако со многими препаратами рибонуклеиновой кислоты не наблюдается количественного распада; по-видимому, присутствует некоторое количество щелочеустойчи-вых связей. Кроме того, так как щелочной гидролиз рибонуклеиновой кислоты включает трансфосфорилирование с образованием промежуточных 2 3 -циклофосфатов, то различия в легкости фосфорилирования 2 -гидроксильных групп нуклеозидов вполне могут отразиться на относительной устойчивости межнуклеотидных связей между различными нуклеозидами. [11]
Так как нас интересует общая нормальность щелочи, а 1 г-экв любой щелочи при диссоциации дает 1 г-ион ОН, можем определить суммарную концентрацию конов ОН независимо от природы исходных щелочей. [12]
Почему не указана природа щелочи. [13]
В системе Li2O - В2О3 - SiO2 эффект увеличения показателя преломления при замене SiOa на В2О3 выражен в 2 - 3 раза слабее, чем в соответствующих натриевой и калиевой системах. Таким образом, влияние природы щелочей на свойства боросиликатных и алюмосиликатных стекол в какой-то мере противоположно. О причинах этого явления будет сказано на стр. [14]
Механизм щелочного активирования изучен недостаточно. По-видимому, он зависит от природы щелочи и от температуры процесса. [15]
Страницы: 1 2