Природа - ионогенная группа
Cтраница 2
Здесь селективность электродной функции, определяемая ЛА-В, не зависит от природы ионогенной группы, а зависит только от энергии сольватации свободных противоионов средой ионита. Поскольку ио-нит ( смоляной) способен к набуханию вводе, то энергия пересольватации не может быть существенной. В этом заключается отличие от жидких ионитов с жидкой органической фазой, практически не растворяющей воду. В последнем случае различие в энергиях пересольватации для разных ионов может быть значительным. [16]
Анализ экспериментальных данных позволяет выявить ряд закономерностей в изменении свойств анионитов в зависимости от природы ионогенных групп матрицы. [17]
Исследования механизма сорбции ионов металлов из растворов ставят задачи, связанные с определением числа активных центров сорбции, их химической природы, а также с выяснением влияния природы ионогенных групп и полимерных матриц сорбентов. [18]
Коэффициент избирательности зависит не только от зарядов обменивающихся ионов и концентрации раствора, но и от других факторов - относительных количеств ионов в ионите и их общей концентрации, химического строения матрицы ионита, природы ионогенных групп и противоионов, температуры. Поэтому, обобщая результаты многочисленных экспериментальных работ во многих трудах по ионному обмену, авторы проводят так называемые ряды сродства или ряды селективности ионов по отношению к ионитам. В этих рядах каждый последующий ион сорбируется сильнее предыдущего. [19]
 |
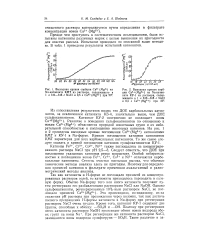
Изотермы адсорбции хлорида натрия на анионите Дауэкс-2 ( / и на. [20] |
Способность ионитов типа змея в клетке поглощать ионы из растворов количественно характеризуется величиной сорбционной емкости. К ним относятся степень поперечной сшитости исходного ионита, природа кислотных и основных ионогенных групп, температура, концентрация раствора, размеры зерен и, что особенно важно, соотношение кислотных и основных групп в грануле. Величина солевой абсорбции является наибольшей в том случае, когда достигнута стехиометрия между содержанием кислотных и основных групп. [21]
По температуре начала и скорости разложения ионогенных групп в воздухе слабоосновные аниониты, у которых ионогенные группы входят в состав матрицы, более термостойки, чем таковые, у которых ионогенные группы находятся в виде боковых заместителей. Начало разложения ионогенных групп в первую очередь зависит, от природы ионогенной группы и молекулярного веса исходного асфальтита. Для получения термостойкого анионита необходимо использовать ароматические амины и высокомолекулярный асфальтит. [22]
Из сопоставления результатов видно, что ДОЕ карбоксильных катио-нитоз, за исключением катионита КБ-4, значительно выше, чем ДОЕ сульфокатионитов. Различие в поведении сульфокатионитов по отношению к йодам Ca2 ( Mg2) объясняется природой ионогенных групп и их избирательной способностью к ( Поглощению некоторых катионов. На рис. 1 и 2 приведены выходные кривые поглощения Ca2 ( Mg2) катионитами КМТ и КУ-1 в Na-форме. Кривая поглощения катионов атионитом КМТ характерна для всех карбоксильных катионитов. [24]
Процесс деионизации водных и водно-органических растворов протекает по описанному выше механизму лишь в редких, простых случаях. Практически он часто бывает осложнен различными взаимодействиями ионов в растворе, например комплексообразова-нием, и во многом зависит от природы ионогенных групп катионита и анионита. [25]
Более детальная трактовка природы изменений смол в результате термической обработки требует разрешения ряда вопросов с применением физико-химических методов исследования. К числу таких вопросов следует отнести выяснение роли воды в процессе десульфирования смол на воздухе, потенциометрическое исследование влияния термической обработки на природу ионогенных групп сульфокатионитов и изучение кинетики обмена ионов водорода в смолах полимеризационного типа на органические ионы большого радиуса. [26]
Для контроля эффективности действия в организме антимикробных волокон проверке также подвергали не содержащие ионогенных групп волокна ( являющиеся исходными при синтезе последних), которые пропитывали теми же антисептиками или антибиотиками, осуществляя сорбционную связь препарата с волокном. Результаты экспериментов представлены в табл. 2, из которой видно, что стойкость антимикробного действия волокон в условиях эксперимента в значительной степени определяется типом связи, природой ионогенных групп и степенью основности антисептика или антибиотика. Так, создание ионной связи между волокном и препаратом позволяет придать материалу более устойчивый антимикробный эффект в сравнении с обычной пропиткой. Причем этот эффект может быть значительно усилен, если осуществлять реакцию ионного обмена между ионообменным волокном и солью четвертичного аммониевого основания, каковой является бриллиантовый зеленый. Однако и в этом случае длительность антимикробного действия этих волокон выше, чем у образцов, импрегнирован-ных растворами антибиотиков. [27]
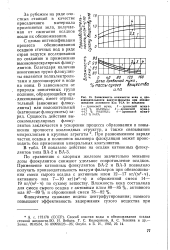 |
Зависимость влажности кека и производительности вакуум-фильтра при обезвоживании активного ила ТСА от введения. [28] |
С целью интенсификации процесса обезвоживания осадков сточных вод в ряде стран ведутся исследования по созданию и применению высокомолекулярных флоку-лянтов. Благодаря наличию ионогенных групп флокулян-ты являются полиэлектролитами и диссоциируют в воде на ионы. В зависимости от природы ионогенных групп полиион, образующийся при диссоциации, имеет отрицательный ( анионные флоку-лянты) или положительный ( катионные флокулянты) заряд. При разноименном заряде частиц осадка и полиионов полимера флокуляция может происходить без применения минеральных коагулянтов. [29]
Поэтому при интерпретации экспериментально найденных констант и проверке уравнений типа ( 12 16) необходимо учитывать механизм переноса заряда в мембране. Например, при симбатном из - менении в ряду катионов ( анионов) специфичности соответствующих электродных функций и энергш связи противоион-фикбированная группа доля специфичности, определяемая сольватационным механизмом, в общем переносе электричества не велика, и она может быть исключена из рассмотрения. Обычно селективность таких электродных систем не велика в силу того, что природа ионогенной группы не оказывает влияния на ее величину. [30]
Страницы: 1 2 3