Прирост - давление
Cтраница 3
Если за меру скорости реакции принять прирост давления Др, то из рисунка видно, что заметное изменение давления начинается лишь с момента времени, равного 64 мин. Отсюда можно заключить, что период индукции равен 64 мин. Если же за меру скорости принять не Ар, а выход формальдегида, то в этом случае как видно из рисунка, период индукции оказывается равным нулю, так как образование формальдегида наблюдается начиная с момента впуска реагирующей смеси в реакционный сосуд. [31]
Формула ( 1) описывает величину прироста давления непосредственно в месте возникновения гидравлического удара. При распространении ударной волны по трубопроводу величина АР постепенно уменьшается вследствие трения. [32]
Формула ( 1) описывает величину прироста давления непосредственно в месте возникновения гидравлического удара. При распространении ударной волны по трубопроводу величина ДР постепенно уменьшается вследствие трения. [33]
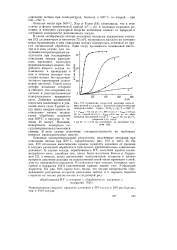 |
Сравнение скоростей реакции окисления метана в сосудах с различно обработанными поверхностями. Смесь 2СН4 О2. 7 5000 С. [34] |
На рис. 109 отложены кинетические кривые прироста давления от времени в сосудах различной обработки и при прочих приблизительно одинаковых условиях. В случае сосуда, обработанного HF, получена кривая несимметричного типа, подобная тем, какие были получены Боном и Гарднером [2], а именно, поело достижения максимальной скорости в начале прироста давления реакция на подавляющей своей части протекает с этой, уже не меняющейся скоростью. В остальных трех сосудах ( старом, прогретом и покрытом РЬО) кинетические кривые имеют уже - образный характер. [35]
 |
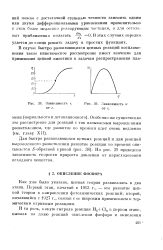
Изменение давления Лр И зависимость lg Др от времени в реакции окисления этана при 610 С ( но данным А. А. Ковальского, П. Я. Са-цикова, Н. М. Чиркова. [36] |
На рис. 93 приведена кинетическая кривая прироста давления Ар в ходе окисления этана. [37]
 |
Зависимость т. [ IMAGE ] Зависимость гл. [38] |
На рис. 39 приведена зависимость скорости прироста давления от израсходования исходного вещества. [39]
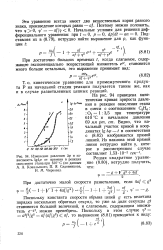 |
Изменение давления Др и зависимость Ig4p от времени в реакции. [40] |
На рис. 94 приведена кинетическая кривая прироста давления в реакции окисления этана в смеси с соотношением С2Не: : О2 1: 3 5 при температуре 610 С и начальном давлении 69 мм рт. ст. Видно, что начальный участок кривой в координатах lg Др - / в соответствии с (8.82) изображается прямой линией. [41]
 |
Зависимость изменения давления Д /. ( / и ig Др ( 2 от времени в реакции окисления этана при 610 С ( по данным Л. А. Коваль ского, П.Я.Садошшкова, Н.М.Чиркова. [42] |
На рис. 108 приведена кинетическая кривая прироста давления Ар в ходе окисления этана. Видно, что начальный участок кривой в координатах In А / 7, t в соответствии с ( VI 1.62) изображается прямой линией. [43]
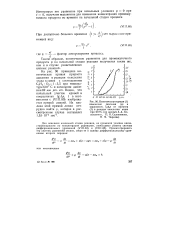 |
Кинетическая кривая ( 1 изменения давления Др и зависимость IgAp от времени ( 2 в реакции окисления этана при 610 С ( по данным А.А. Ковальского, П.Я. Садовникова, Н, М. Чиркова. [44] |
На рис. 96 приведена кинетическая кривая прироста давления в реакции окисления этана в смеси с соотношением С2Н8: О21: 3 5 при температуре 610 С и начальном давлении 69 мм рт. ст. Видно, что начальный участок кривой в координатах lg Ар, t в соответствии с ( VIII. [45]
Страницы: 1 2 3 4 5