Присоединение - бензольное кольцо
Cтраница 1
Присоединение бензольного кольца к алкильной группе значительно облегчает кислотную диссоциацию соседней С 3 - Н - связи и обеспечивает тем самым повышенные кислотные свойства соответствующего углеводорода. Значения рКа слабых кислот, какими в общем являются углеводороды, измеряют в специальных условиях с применением сверхсильных оснований, а затем пересчитывают полученные значения, приводя их к шкале, в которой вода служит стандартным растворителем. [1]
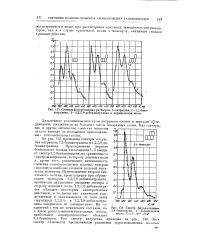 |
Спектры флуоресценции растворов. 1-антрацена, 2 - 1 2-бенз.| Спектр флуоресценции 3 4-бензпирсна л парафиновом масле. С3 10 - 4 г /. [2] |
Присоединение первого бензольного кольца в положения 1, 2 смещает спектр 1 2-бензантрацена, по сравнению со спектром антрацена, в сторону длинных волн и, кроме того, увеличивает интенсивность свечения коротковолновой полосы, которая становится наиболее сильной полосой излучения молекулы. Присоединение второго бензольного кольца, происходящее при образовании молекулы 1 2 5 6-дибензантрацена, производит дальнейшее смещение спектра в сторону длинных волн. Из соединений с тем же химическим составом, но с иным расположением бензольных колец, наибольшей канцерогешюстью обладает 3 4-бензпирен. Этот спектр отличается чрезвычайным развитием коротковолновой полосы. [3]
Ангулярное присоединение бензольного кольца в положении 1 2 аценов сопровождается повышением энергии Г - состояния или уменьшением величины SI, Т - интервала. Для более многоядерных аценов: 1 2-бензтетрацена ( IX) и 1 2-бензпентацена описаны лишь спектры поглощения; длинноволновые полосы по положению и колебательной структуре довольно сходны с полосами спектров исходных аценов. [4]
Рассмотрим теперь ангулярные молекулы с центрально-симметричным присоединением бензольных колец. [5]
Сульфирование бензольного кольца стирола может идти в орто -, мета - или пара-положение к месту присоединения бензольного кольца к углеводородной цепи. Поэтому в одном бензольном кольце могут существовать три различных типа сульфо-групп. Кроме того, бензольные кольца ДВБ также сульфируются и приводят к шести дополнительным изомерам по сульфогруппам. Если в ДВБ присутствует этилстирол, то можно получить более десяти изомерных соединений по сульфогруппам. [6]
Скорость, с которой алкилбензолсульфонаты окисляются микроорганизмами, кроме обратной зависимости от числа углеродных атомов между конечной метильной и сульфонатной группами зависит также и от места присоединения бензольного кольца. Установлено, что 2-фенилизомер разрушается наиболее быстро, затем идут 3 4 и 5-фенилизомеры. [7]
Сложность состава фракций высокомолекулярных алкилфено-лов определяется различием в длине и строении алкильного радикала, различием в числе и положении алкильных радикалов по отношению к гидроксильной группе в бензольном кольце и различием в положении места присоединения бензольного кольца к одному из углеродных атомов алкильного радикала, а также наличием алкилфениловых эфиров и не вошедших в реакцию углеводородов и фенола. Для более высокомолекулярных алкилфенолов необходимо комплексное использование методов препаративного разделения и анализа, включая кроме вышеукаганных методов жидкостную адсорбционную хроматографию, а также ядерно-магнитный резонанс. [8]
Таким образом, основную часть летучих компонентов пеков составляют ПАУ с конденсированными ядрами; присутствуют также соединения, содержащие в конденсированной ароматической системе тиофеновое или фурановое кольцо. Можно выделить несколько основных рядов бензологов, образованных присоединением бензольных колец к исходной ароматической системе: антраценовые - фенантреновые ( mlz 178 - 228 - 278 - 328 - 378 - 428 - 478), пиреновые ( 202 - 252 - 302 - 353 - 402), флуорантеновые ( 226 - 276 - 300 - 326 - 376 - 426), тио-феновые ( 234 - 284 - 334 - 384), фурановые ( 218 - 268 - 318) и др. Следовательно, при увеличении молекулярных масс ароматических полициклических компонентов пеков структура их изменяется либо путем присоединения к определенным ароматическим ядрам дополнительных бензольных колец, либо путем образования более протяженных ядер, составленных из плоской сетки бензольных колец разной конфигурации. [9]
При присоединении к такого рода молекуле бензольного кольца число ic - электронов возрастает на 4, и молекула остается в классе аномальных молекул. Поэтому бензо-гомологи вышеупомянутых молекул должны также обнаруживать аномальный парамагнетизм. Однако присоединение бензольных колец все же увеличивает число полностью занятых дублетных уровней в молекуле и должно приводить к количественной убыли парамагнетизма u - электронов за счет увеличения суммарного диамагнитного вклада. [10]
Метод основан на том, что алкилбензолсульфонаты в смеси с Р2О5 или Н3Р04 подвергают пиролизу в токе инертного газа при 400 - 550 С. В этих условиях связи С-S быстро расщепляются, тогда как связи С-С расщепляются сравнительно слабо или практически не расщепляются. Продукты пиролиза анализируют методом газо-жид-костной хроматографии, по полученным хроматограммам рассчитывают количественное распределение гомологов и изомеров по месту присоединения бензольного кольца к алкильному радикалу в гидрофобной части линейных алкилбензолсульфонатов. [11]
Фракции этих ПФ с молекулярным весом 2000 - 3000 плавятся при 300 - 400 С. Полимеры, полученные на основе би-фенила, менее стабильны. Высокая термостабильность линейного ПФ, бензольные кольца которого соединены между собой в пара-положении, не является неожиданной. Известно, что различные типы присоединения бензольных колец ( мета -, орто - или пара -) могут приводить к различным эффектам. [12]
Страницы: 1