Присоединение - третье - атом
Cтраница 1
 |
Результаты квантовомеханического расчета молекулы водорода. [1] |
Присоединение третьего атома к молекуле Н2 невозможно, поскольку условием для перекрывания электронных облаков, которое дает химическую связь, является наличие у электронов антипараллельных спинов. Спин электрона третьего атома водорода неизбежно будет совпадать по направлению со спином одного из электронов в молекуле. Поэтому между третьим атомом водорода и молекулой водорода будут действовать силы отталкивания, подобные тем, которые появляются при сближении двух атомов водорода с параллельными спинами. [2]
Присоединение третьего атома невозможно, так как тогда на этом уровне нужно было бы уместить три электрона, два из которых, очевидно, должны были бы иметь одинаковые спины, что противоречит принципу Паули. Третий электрон мог бы поместиться лишь на одном из уровней следующего L-слоя ( п - 2), но для такого перехода нужна была бы невозможно большая затрата энергии. Таким образом, молекула Нз не может образоваться. [3]
 |
Строение валентного электронного уровня атома кремния в молекуле SiF.. [4] |
Так, присоединение третьего атома фтора сопровождается заметным понижением количества выделяющейся энергии. Очевидно, часть энергии, получающейся при образовании связи, расходуется на промотирование электрона. [5]
Гейтлера и Лондона и, следовательно, насыщаемости ковалентной связи сводится: к тому, что присоединение третьего атома водорода к молекуле Н2 невозможно, так как его спин будет обязательно совпадать со спином одного из двух электронов молекулы. Поэтому между третьим атомом водорода и Н2 будут действовать силы отталкивания, в результате никакого перекрывания электронных облаков не может быть. [6]
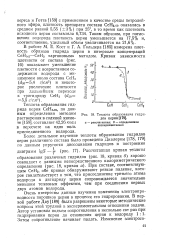 |
Теплота образования гидридов церия. [7] |
При составе, соответствующем СеН2, обе кривые обнаруживают резкое падение, которое свидетельствует о том, что присоединение третьего атома водорода к дигидриду церия сопровождается значительно меньшим тепловым эффектом, чем при соединении первых двух атомов водорода. [8]
Если остановить ферментативную реакцию, то после деградации фермента удается получить небольшое количество 5 -дезок-сиаденозина, образующегося из лиганда путем присоединения третьего атома водорода в положение Сз -, что также подтверждает разрыв связи Со-С. [9]
 |
Результаты квантовомеханического расчета молекулы водорода. [10] |
Не рассматривая данный расчет, можно пояснить его результат исходя из того, что было сказано выше о результатах расчета молекулы Н2 - Присоединение третьего атома к молекуле Н2 невозможно, поскольку условием для перекрывания электронных облаков, которое дает химическую связь, является наличие у электронов антипараллельных спинов. Поэтому между третьим атомом водорода и молекулой водорода будут действовать силы отталкивания, подобные тем, которые появляются при сближении двух атомов водорода с параллельными спинами. [11]
Так было дано теоретическое обоснование важнейшего свойства ковалентной связи - насыщаемости. Присоединение третьего атома к Н2 не происходит, поскольку условием для перекрывания электронных облаков, которое дает химическую связь, является наличие у электронов антипараллельных спинов. Спин электрона третьего атома водорода неизбежно будет совпадать по направлению со спином одного из электронов в молекуле. [12]
Насыщаемость - свойство атомов образовывать строго определенное число ковалентных связей. Например, в молекуле водорода химическая связь осуществляется парой электронов, имеющих противоположные спины. Присоединение третьего атома к молекуле Н2 исключается ввиду того, что его спин обязательно совпадает со спином одного и двух электронов в двухатомной молекуле. [13]
Например, в молекуле водорода химическая связь осуществляется парой электронов, имеющих противоположные спины. Присоединение третьего атома к молекуле Н2 исключается ввиду того, что его спин обязательно совпадает со спином одного из двух электронов в двухатомной молекуле. [14]
Представление о перекрывании электронных облаков соседних атомов и обменном направленном взаимодействии двух электронов с антипараллельными спинами составляют основу современной теории строения молекул. Действительно, к молекуле водорода не может присоединиться еще один атом водорода, так как спин его электрона параллелен спину одного из электронов, входящих в молекулу водорода, и между ними возникнут силы отталкивания, препятствующие присоединению третьего атома. [15]
Страницы: 1 2