Присоединение - азот
Cтраница 1
Присоединение азота к свободной электронной паре представляет собой довольно редкую реакцию. [1]
Присоединение азота воздуха к карбиду кальция с образованием цианамида, из которого затем получается аммиак гидролизом. [2]
После присоединения азота происходит смена коллоидного носителя и начинается восстановление продукта фиксации азота подвижным водородом, мобилизуемым дегидразами из окисляемого органического вещества. [3]
Происходит ли присоединение азота к Cs или С1 ( зависит не только от строения веществ, участвующих в реакции, но и от условий опыта. [4]
Во-первых, следует отметить, что присоединение азота по второму углеродному атому тройной связи затруднено прежде всего потому, что электронодонорное влияние алкильных групп дестабилизирует анион, образующийся на соседнем углеродном атоме. Во-вторых, устойчивость цикла ( хТТУ) должна быть гораздо меньше, поскольку он содержит большее количество атомов водорода и, следовательно, дестабилизирован по сравнению с ( ххт) за счет трансаннуляр-ного отталкивания протонов. [5]
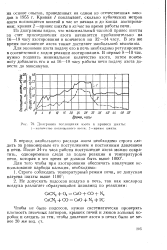 |
Диаграмма поглощения азота и привеса шихты. / - количество поглощенного азота. 2 - привес шихты. [6] |
Из диаграммы видно, что максимальный часовой привес шихты за счет присоединения азота начинается приблизительно на 16 - 18 часу азотирования и кончается на 32 - 34 часу. В это же время поглощение азота также достигает наибольшей величины. [7]
В этой работе предполагается, что основная стадия процесса при низкой температуре состоит в присоединении азота к молекуле углеводорода. Вероятно, что реакции такого типа не будут определяющими в плазменном процессе, так как при высоких температурах предельные углеводороды отсутствуют. [8]
Лактамы - это циклические аналоги амидов с открытой цепью; их называют р -, у или 6-лактамами в зависимости от места присоединения азота к углеводородной цепи. [9]
Сродство низковалентных металлов к молекулам воды может быть в ряде случаев значительно меньшим, чем к молекулам водорода, азота, углеводородов, по-видимому, из-за прочности связи Н - ОН и из-за отсутствия двойной или тройной связи, что не позволяет осуществить дативного взаимодействия, как в случае присоединения азота. Известно, что молекулы воды входят в координационную сферу металлов, но, как оказывается для некоторых низковалентных металлов, эта координационная связь очень непрочна и может замещаться, например, молекулярным азотом. Поэтому реакции низковалентных производных металлов с молекулами водорода, углеводородов и азота становятся возможными в водных средах. Именно эти элементарные реакции, по всей вероятности, используются живыми организмами, способными усваивать азот, водород, углеводороды, для активации этих молекул. [10]
Будучи реакцией обратимой, переаминирование обычно служит начальным этапом катаболизма избыточных аминокислот. В результате присоединения азота к кето-глутарату образуется избыточный глутамат, который дезаминируется с образованием аммиака и далее - глутамина. Глутамин может также отдавать свой азот на образование аспартата. В организме животного и аспартат, и глутамин ( через карбамоилфосфат) являются предшественниками мочевины, главного экскреторного азотистого соединения. Все эти взаимосвязи суммированы в уравнении ( 14 - 12), а дальнейшие подробности будут даны в последующих разделах. [11]
Стерически ненапряженные аминовые комплексы ВНз и BF3 обычно при комнатной температуре являются твердыми веществами; на них слабо влияют влага и кислород воздуха. Четвертая связь при атоме бора, образованная в результате присоединения азота, заметно стабилизирует бораны ВН3 и ВРз. Хотя большинство амин-боранов в твердом состоянии недостаточно хорошо изучено, обычно полагают, что эти соединения являются простыми веществами определенного состава. Для: соединений H3NBH3 [29], H3BNF3 [30], CH3H2BNH3 [30] ( CH3) 2HNBH3 [30] и ( CH3) 3NBF3 [31] молекулярные веса в жидком аммиаке согласуются с мономерными формулами. В бензольных растворах наблюдается значительная ассоциация, что объясняют небольшой диэлектрической проницаемостью растворителя. [12]
Взаимодействие происходит уже при смешении на вальцах. При повышении температуры ( более 60 С) становится заметным распад продуктов нитрования, хотя присоединение азота к каучуку идет с большей скоростью. [13]
Поскольку цианамид кальция получают при взаимодействии газообразного азота с твердым карбидом кальция, естественно, для более полного протекания реакции необходимо, чтобы площадь соприкосновения этих двух реагирующих веществ была максимальной. Поэтому карбид кальция дробят и размалывают до тонкого порошка в специальных шаровых мельницах. В качестве катализатора, ускоряющего процесс азотирования - присоединения азота, к карбиду кальция добавляют 2 - 3 процента плавикового шпата ( CaF2) и другие соединения. [14]
Страницы: 1