Присутствие - избыток - водяной пар
Cтраница 1
Присутствие избытка водяного пара весьма неблагоприятно сказывается на прочности катализатора: он размягчается и деформируется, спрессовываясь в сплошную массу еще до полной потери активности. Рост перепада давления в реакторе ведет к вынужденному прекращению работы. Выгрузка отработанного катализатора чрезвычайно затруднена, и ее приходится производить с помощью специальных высверливающих устройств. [1]
Присутствие избытка водяного пара, по-видимому, не влияет на окисление сероводорода до сернистого ангидрида. [2]
Как показали исследования Оболенцева, процесс изомеризации проходит в присутствии избытка водяного пара, препятствующего полимеризации бутиленов. [3]
Отложение углерода не является главной проблемой для катализаторов конверсии СО последующим причинам: присутствие избытка водяного пара предотвращает выделение углерода, а окисленное состояние железа в железохромовых катализаторах делает их неактивным в реакции Будуара. [4]
 |
Сопоставление температурной зависимости свободных энергий образования гидроокисей щелочноземельных. [5] |
Вообще же летучесть всех гидроокисей в щелочноземельных металлах заметно меньше, чем для щелочных, и измеряется в интервале 1500 - 3500 К малыми долями мм рт. ст. В присутствии избытка водяного пара под давлением испарение несомненно значительно облегчается. [6]
Известно, что металлические Fe, Co и Ni катализируют полное разложение углеводородов до кокса и водорода. Поэтому для предупреждения восстановления окиси железа до металла необходимо проводить реакцию в присутствии избытка водяного пара. Условия использования катализатора 1707 и его модификаций следующие: 1 - 2 бар, 550 - 800 С, 100 - 800 ч 1, олефин: Н2О 1: 7 - 1: 15 ( мол. [7]
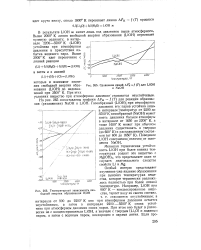 |
Сравнение линий и NaOH.| Температурная зависимость свободной энергии образования КОН. [8] |
В результате LiOH ж кипит лишь под давлением выше атмосферного. Выше 2000 К линия свободной энергии образования ( LiOH) пересекает нулевую ординату; в интервале 2200 - 3500 К ( LiOH) устойчива при атмосферном давлении в присутствии избытка водяного пара. [9]
Хлорид бериллия можно также отнести к последней группе, хотя точных данных о давлении его пара не имеется. Давления паров фторидов этих металлов могут относиться друг к другу подобным же образом, хотя давления паров фторидов должны отличаться по своему абсолютному значению от соответствующего хлорида. Склонность А1С13 ( и, возможно, A1FS) к гидролизу в присутствии избытка водяного пара [22], вероятно, препятствует его транспортировке на большие расстояния в газообразной фазе. С другой стороны, Циис [25] ссылается на экспериментальное подтверждение того факта, что железо может быть перенесено в виде хлоридов в газообразном состоянии, несмотря на различие между давлением паров FeCl2 и FeCl3, и что когда оба хлорида при температуре, близкой к 550, будут вступать в реакцию с водяным паром, то будет образовываться магнетит. Происхождение части магнетита Железной горы, образовавшегося в течение ранних высокотемпературных стадий тогда, когда магма активно проникала в окружающую породу, можно объяснить аналогичными реакциями фторидов. [10]
Однако при такой температуре скорость реакции окисления метана водяным паром очень мала. Реакция протекает с значительной скоростью лишь при температурах 1350 С и выше. Из-за трудности ведения эндотермического процесса при столь высоких температурах в промышленных условиях процесс паровой конверсии метана ведут на катализаторе в присутствии избытка водяного пара по сравнению со стехиомет-рическим количеством. В табл. 11 приведен рассчитанный Б. П. Корниловым равновесный состав газовой смеси, образующейся в процессе паровой конверсии метана при различных температурах и давлениях и соотношении СН: Н2О1: 2 в исходной газовой смеси. [11]
Данные табл. 12 показывают, что выше 900 реакция ( 1) протекает практически до конца. Теоретически реакция ( 3) при этих температурных условиях также должна проходить полностью. Однако, поскольку для сдвига реакции ( 2) вправо высокая температура неблагоприятна, основным углеродистым соединением при этих условиях даже в присутствии избытка водяного пара является окись углерода. [12]
Данные табл. 12 показывают, что выше 900 реакция ( 1) протекает практически до конца. Теоретически реакция ( 3) при этих температурных условиях также должна проходить полностью. Однако, поскольку для сдвига реакции ( 2) вправо высокая температура неблагоприятна, основным углеродистым соединением при этих условиях даже в присутствии избытка водяного пара является окись углерода. [13]
Страницы: 1