Присутствие - ион - железо
Cтраница 2
В присутствии ионов железа автоокисление фруктозы активируется пиро-фосфатом, а автоокисление цистеина тормозится. [16]
В присутствии ионов железа ( III) к исследуемому и эталонному растворам добавляют по 5 капель фосфорной кислоты с целью маскирования ионов железа, мешающих определению титана. [17]
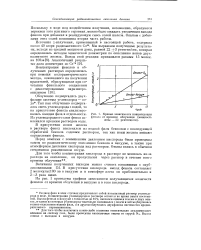 |
Кривые зависимости концентрации. [18] |
В присутствии ионов железа в растворе фенол извлекался из водной фазы бензолом с последующей обработкой бензола содовым раствором, так как ионы железа мешают определению фенола. [19]
В присутствии ионов железа ( III), чтобы предотвратить образование в аммиачном растворе гидроокиси железа, к анализируемому раствору предварительно добавляют сегнетову соль или NH4F для связывания Ре - ионов в комплексный ион. [20]
В присутствии ионов железа ( III) образуются окрашенные внутрикомплексные соли трехвалентного железа. [21]
В присутствии ионов железа ( II), являющихся катализатором процесса окисления хлорид-ионов перманганатом, результаты титрования получаются неправильными ( см. Железо, стр. [22]
В присутствии ионов железа ( III), чтобы предотвратить образование в аммиачном растворе гидроокиси железа, к анализируемому раствору предварительно добавляют сегнетову соль или NH4F для связывания Fe - ионов в комплексный ион. [23]
В присутствии ионов железа ( III) к исследуемому и эталонному растворам добавляют по 5 капель фосфорной кислоты с целью маскировки ионов железа, мешающих определению титана. [24]
В присутствии ионов железа ( Fe3) свечение постепенно ослабевает. Окислители ( перекись водорода, бихроматы) и восстановители ( тиосульфат, гидроксиламин, аскорбиновая кислота) соответственно ускоряют и замедляют исчезновение флуоресценции реагента. Соотношение концентраций реагента и ионов железа, при котором происходит исчезновение флуоресценции, около 1000: 1; поэтому наиболее вероятной причиной гашения флуоресценции является окисление реагента, каталитически ускоряемое ионами железа. [25]
В присутствии ионов железа ( III), чтобы предотвратить образование в аммиачном растворе гидроксида железа, к анализируемому раствору предварительно добавляют сегнетову соль или NH4F для связывания Ре3 - ионов в комплексный ион. [26]
В присутствии ионов железа и легко окисляемых органических веществ оплывание тоже может усилиться. Если их окисление будет происходить за счет саморазряда положительной активной массы ( во время отсутствия заряда) на самой поверхности электрода, то образовавшийся сплошной слой сульфата свинца может при заряде дать плохо связанный с основной массой слой РЬО2, который оплывет. [27]
В присутствии ионов железа ( Fe3) свечение постепенно ослабевает. Окислители ( перекись водорода, бихроматы) и восстановители ( тиосульфат, гидроксиламин, аскорбиновая кислота) соответственно ускоряют и замедляют исчезновение флуоресценции реагента. Соотношение концентраций реагента и ионов железа, при котором происходит исчезновение флуоресценции, около 1000: 1; поэтому наиболее вероятной причиной гашения флуоресценции является окисление реагента, каталитически ускоряемое ионами железа. [28]
Испытание на присутствие ионов железа ( II) и железа ( III) проводят из всей смеси до проведения разделения. [29]
Разложение перекиси ускоряется в присутствии ионов железа, меди, марганца, кальция, поэтому в пере-кисные растворы в качестве стабилизаторов добавляют силикат натрия и сернокислый магний. [30]
Страницы: 1 2 3 4