Присутствие - иттрие
Cтраница 1
Присутствие иттрия в паровой фазе впервые было обнаружено при 1600 К. [1]
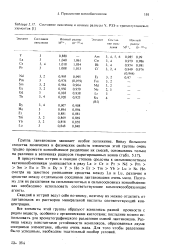 |
Состояние окисления и ионные радиусы Y, РЗЭ и трансплутониевых элементов. [2] |
В присутствии иттрия и скандия степень сродства к сильнокислотным катионообменникам уменьшается в ряду La Се Рг Nd Pm Sm Eu Tb Dy Y Но Er Tm Yb Lu Sc. Несмотря на заметное уменьшение сродства между La и Lu, различие в сродстве между отдельными соседними лантаноидами очень мало. Поэтому для их разделения на сильнокислотных и сильноосновных ионообменни-ках необходимо использовать соответствующие комплексообразующие агенты. [3]
Для определения в присутствии иттрия скандий гидролизуют при рН 6 3 и определяют в фильтрате иттрий. Вначале титруют все компоненты, включая скандий, а затем, после введения NH4F, титруют ЭДТА, выделившуюся в количестве, эквивалентном содержанию скандия. [4]
Для определения в присутствии иттрия скандий гидролизуют при рН 6 3 и определяют в фильтрате иттрий. [5]
Предложен фотометрический метод определения лантана в присутствии иттрия при использовании маскировки реакции иттрия фторидом натрия и метод определения иттрия в смеси с лантаном, основанный на способности сульфата натрия снижать интенсивность окраски комплекса лантана в большей степени, чем иттрия. [6]
Показана возможность использования метода для определения стронция в присутствии иттрия. Относительная ошибка определения 5 - 10 %, продолжительность 20 - 30 минут. [7]
Ряд методов отличается высокой избирательностью и позволяет определять скандий в присутствии иттрия и лантанидов. [8]
Метод основан на осаждении скандия в виде основного тар-трата в присутствии иттрия в качестве соосадителя. Осадок прокаливают, растворяют в соляной кислоте и определяют скандий фотометрически при помощи сульфоназо. [9]
Поэтому скандий не является элементом преимущественно магматических остаточных щелоков, как рзэ, а концентрируется в силикатах, богатых магнием и железом. Если присутствие иттрия обязательно во всех редкоземельных минералах, содержащих иттриевую подгруппу элементов, то о скандии этого сказать нельзя. [10]
При снижении рН до 2 0 мешающее влияние большинства перечисленных металлов ослабевает, а иттрий вообще не оказывает влияния. Согласно Белопольскому и Попову [4], в присутствии иттрия получаются все же несколько завышенные результаты определения скандия; поэтому они рекомендуют в растворы, применяемые для построения калибровочного графика, вводить примерно такие же количества иттрия, какие содержатся в анализируемом растворе. [11]
Многие элементы ведут себя аналогично. Прямолинейная зависимость интенсивности свечения от концентрации наблюдается в пределах от 0 2 до 6 0 мкг / мл. При введении в анализируемый раствор иона фтора возможно определение скандия в присутствии иттрия и суммы редкоземельных элементов по разности свечения растворов, так как фтор-ион, гася люминесценцию окси-хинолината скандия, не влияет на люминесценцию иттрия и суммы редкоземельных элементов. Для этого вначале измеряют суммарную люминесценцию скандия и суммы редкоземельных элементов, а затем, после добавления фторида, свечение иттрия и редкоземельных и по разности определяют содержание скандия. [12]
Для обнаружения лантанидов в окиси кальция последнюю, в виде королька, прокаливают в верхней части пламени в течение 2 мин. Королек охлаждают 2 - 3 мин и вносят в нижнюю часть пламени. Если в окиси кальция имеются лантаниды, возникает люминесценция. Если же в препарате присутствует несколько примесей, то они светят в разных местах королька, так как оптимальная температура активации разных примесей различна. Желто-зеленым цветом люминесцируют церий, самарий и тулий, зеленым - диспрозий, люминесценция красного цвета различных оттенков возникает в присутствии лантана, празеодима и неодима и сине-фиолетового-в присутствии иттрия. Автор указывает, что метод настолько чувствителен, что позволяет обнаруживать 1 10 - 8 г иттрия в 1 г окиси кальция, а так как масса королька в опытах равнялась 0 1 г, то абсолютная чувствительность метода составляла 0 001 мкг иттрия. [13]
Страницы: 1