Присутствие - свободная кислота
Cтраница 3
Кислая среда указывает на присутствие свободных кислот; щелочная среда указывает на присутствие свободных основании; нейтральная среда указывает на отсутствие свободных кислот и оснований. [31]
Кислая среда указывает на присутствие свободных кислот; щелочная среда - на присутствие свободных оснований; которые даны для анализа или образовались в результате гидролиза; нейтральная среда указывает на отсутствие свободных кислот и оснований. [32]
Избыток кислоты по отношению к количеству кислоты, связанной со свинцом, необходим для предупреждения гидролиза соли свинца повышения электропроводности раствора. Кроме того, в присутствии свободной кислоты несколько повышается катодная поляризация и улучшается структура осадка. Несмотря на повышенную кислотность электролитов, выход металла по току в рабочем интервале плотностей тока составляет 100 %, что объясняется высоким перенапряжением водорода на свинце и сравнительно малой катодной поляризацией при выделении свинца. [33]
Они встречаются в гранате, где много свободной кремнекислоты. Непонятно происхождение основной соли в присутствии свободной кислоты и в тех обстоятельствах, когда образуется рядом средняя соль. Напротив того, если признать слюду и гранат за соли средние, то будет понятно, почему в присутствии избытка кислоты образуется ( полевой шпат) кислая соль. [34]
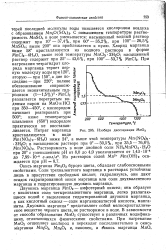 |
Изобара диссоциации МпО2. [35] |
Окись марганца Мп2Оз бурого цвета, обладает слабоосновными свойствами. Соли трехвалентного марганца в растворах устойчивы лишь в присутствии свободных кислот; гидролизуясь, они дают осадок гидратированной окиси марганца или соли двухвалентного марганца и гидратированную двуокись марганца. [36]
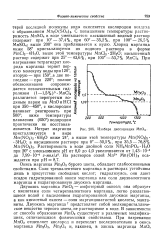 |
Изобара диссоциации МпОа. [37] |
Окись марганца Мп2О3 бурого цвета, обладает слабоосновными свойствами. Соли трехвалентного марганца в растворах устойчивы лишь в присутствии свободных кислот; гидролизуясь, они дают осадок гидратированной окиси марганца или соли двухвалентного марганца и гидратированную двуокись марганца. [38]
Кубовые красители переходят из щелочного раствора их лейкосоединений на волокно и там образуются в результате окисления. Этот процесс может вызываться кислородом воздуха или другими окислителями в присутствии свободных кислот. В качестве куба теперь применяется преимущественно кислый сульфитный куб; он содержит, кроме кислого сульфита и красителя, едкую щелочь, глауберову соль или сернокислый аммоний. Искусственное окисление производится хромовыми солями, пер-борнокислым натрием или перекисью водорода. При сильном разбавлении куба и нехватке кислого сульфита красители выделяются в осадок. В сточных водах обычно имеются эти условия. [39]
Заметив, что надхромовая кислота в эфирном растворе легко превращает в присутствии свободной кислоты анилин в фиолетовый краситель, я пытался использовать эту реакцию для обнаружения перекиси водорода, применяя раствор двухромовокислого калия, к которому прибавлен анилин и кислота. Как известно, двухромовокислый калий сам по себе способен превратить в присутствии свободной кислоты анилин в фиолетовый краситель. Однако, ввиду малой устойчивости надхромовой кислоты, можно было рассчитывать, что в очень разбавленных растворах ее действие на анилин обнаружится значительно раньше, чем действие двухромовокислого калия. Действительно, в очень разбавленном растворе двухромовокислого калия, содержащем анилин и щавелевую кислоту, я наблюдал фиолетово-розовое окрашивание при малейших следах перекиси водорода, в то время как в ее отсутствии раствор оставался неизмененным в течение нескольких часов. [40]
Изучена скорость изотопного обмена водорода в растворах азотнокислого, сернокислого и хлористого аммония. Показано, что этот обмен протекает в воде с измеримой скоростью и значительно замедляется в присутствии свободных кислот. [41]
Солянокислая соль бензидина легко растворима в воде, еще легче растворима в алкоголе и почти нерастворима в эфире. Из водных и алкогольных растворов она кристаллизуется в виде белых с серебристым блеском тонких ромбических листочков, которые не изменяются в сухом и даже во влажном состоянии; при соприкосновении с эфиром, особенно на воздухе или в присутствии свободной кислоты, соль разлагается: она окрашивается в грязно-зеленый цвет и теряет свою кристаллическую форму. [42]
Вначале смешивают в кипящем метаноле водные растворы гексаметилендиамина и адипиновой кислоты. При охлаждении выпадает соль АГ, которую очищают перекристаллизацией и сушат. Присутствие свободной кислоты или амина может вызвать расщепление цепи, а также блокирование растущей цепи, что снижает молекулярный вес полимера. Для регулирования молекулярного веса продукта специально добавляют определенное количество свободных диаминов и дикарбоновых кислот. [43]
Навеску вещества растворяют в воде и титруют раствором азотнокислого серебра, применяя в качестве индикатора хромовокислый калий. Присутствие свободной кислоты мешает титрованию, так как красный осадок хромовокислого серебра растворим в кислоте, и при этом нельзя установить точку эквивалентности. Кислые растворы нейтрализуют перед титрованием, прибавляя к ним кислый углекислый натрий. [44]
Механизм процесса в основном не отличается от рассмотренного при рафинировании меди ( стр. Напомним, что детали процесса определяются наличием ионов закисной и окисной меди. Присутствие свободной кислоты несколько снижает активность ионов меди, делает осадок более мелкокристаллическим и мягким; кроме того, повышает электропроводность и препятствует выпадению основных закисных солей меди. Но слишком большой избыток серной кислоты может вызвать растворение катоднвй меди. Повышение температуры увеличивает размеры кристаллов меди, но зато позволяет повысить плотность тока, что, в свою очередь, ведет к мелкокристалличности осадка и парализует влияние температуры. [45]
Страницы: 1 2 3 4