Присутствие - 100-кратное количество
Cтраница 2
К а д и о н в капельном варианте позволяет открывать кадмий ( открываемый минимум 0 1 мкг, С 3 2 мкг / мл; уверенно открываемый минимум - 0 3 мкг, С - 10 мкг / мл) в присутствии 100-кратных количеств As, Аи, Bi, Mo, Pb, Pt Sb, Se, Sn, Те, Tl, V, W и Zn. Ионы Со, Cr, Си и Ni дают синеватую окраску, Mg - синюю, a Fe - желтую, что несколько затрудняет обнаружение кадмия; но их можно замаскировать тартратом. В этом случае на фильтровальную бумагу помещают каплю нейтрального или слабо уксуснокислого испытуемого раствора и прибавляют по капле 10 % - ного раствора сегнетовой соли, 0 02 % - ного спиртового, содержащего 0 02 N КОН, раствор реагента и 2 N раствор КОН. В присутствии кадмия появляется розовое пятно, без него бумага окрашивается в фиолетовый цвет. [16]
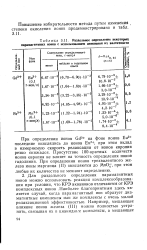 |
Раздельное определение некоторых парамагнитных ионов с использованием изменения их валентности. [17] |
При определении ионов Gd3 на фоне ионов Еи2 последние окислялись до ионов Еи3, при этом вклад в измеряемую скорость релаксации от ионов европия резко снижался. Присутствие 100-кратных количеств ионов европия не влияет на точность определения ионов гадолиния. При определении ионов трехвалентного железа ионы марганца ( II) окисляются до МпО -, при этом любые их количества не мешают определению. [18]
 |
Кристаллы K2Pb [ Cu ( N02 6 ]. [19] |
Соли аммония ( а также рубидия и цезия) дают аналогичные осадки с платинохлористоводородной кислотой и мешают обнаружению катионов калия. Присутствие 100-кратных количеств ионов натрия не мешает. [20]
В присутствии га-нитроанилина появляется розовая или красная окраска. Реакция позволяет обнаружить n - нитроанилин в присутствии 100-кратного количества обоих его изомеров. [21]
Гидрон II является чувствительным реагентом на ионы кальция; открываемый минимум составляет 0.1 мкг Са / мл. Титрование кальция с этим индикатором возможно и в присутствии 100-кратных количеств магния. При наличии большого количества магния рекомендуется возможно большее разбавление раствора и тщательное перемешивание его в процессе титрования. Титруют немедленно после прибавления щелочи; в противном случае сорб-ционные процессы ухудшают фиксирование точки эквивалентности и понижают точность результатов анализа. Методика определения кальция в присутствии магния сводится к следующему. [22]
Титрование проводят в 7 - 10 % - ной соляной, 15 - 30 % - ной хлорной, 10 - 12 % - ной серной или 50 % - ной фосфорной кислотах. При определении этим методом 0 1 - 100 мг соли гидразина получаются хорошие результаты даже в присутствии 100-кратных количеств нитратов и солей аммония. Определению мешают мочевина и гидроксил-амин. [23]
Определение индия при рН 2 3 - 2 5 выполнено в присутствии 20-кратных количеств цинка, 50-кратных - кадмия, 25-кратных - марганца и кобальта, 100-кратных - ртути и фосфата-ионов. Ионы сульфат - и арсенат - значительно снижают интенсивность люминесценции; однако при рН 2 3 возможно присутствие 100-кратных количеств сульфат-ионов, при увеличении рН до 2 5 - 2 8 и концентрации морина можно определять индий в присутствии 50-кратных количеств арсенат-ионов. [24]
Без добавки некоторых реагентов потребляется избыточное количество AgNO3 для титрования иодида; в аммиачном растворе результаты точные. Точные результаты получаются также и без добавки аммиака при интенсивном помешивании, если только J -: Br - 1: 50.10 В присутствии 100-кратного количества бромида. [25]
Со и Те ( по сравнению с содержанием Zn или Cd) происходит гашение флуоресценции. Такой же эффект вызывает присутствие 100-кратных количеств ионов Li, Fe-2, Fe 3, Gd, Sb 3, Hg. При содержании в растворе посторонних катионов в количестве, не превышающем количество цинка или кадмия, гашения не происходит. [26]
Через несколько минут проволоку извлекают из капилляра, сушат и нагревают в маленькой трубке, после чего стенки трубки рассматривают под микроскопом. Нагревать следует только нижнюю часть трубки. Такой способ выполнения испытания позволяет заметить капельки ртути еще при 0 2 fHg в присутствии 100-кратного количества серебра. [27]
Электроды на основе мембран с подвижными носителями имеют жидкие мембраны - раствор ионообменника или нейтрального переносчика в органическом растворителе, удерживаемый на пористом полимере ( рис. IV. Органический растворитель влияет на свойства электрода. Так, если для растворения кальциевой соли эфира фосфорной кислоты [ ( КСЬЬРООЬСа используют диоктилфенилфосфонат, то электрод пригоден для определения ионов кальция в присутствии 100-кратного количества магния. Но если растворителем является деканол-1, то электрод не способен различить кальций или магний; его можно, однако, использовать для определения жесткости воды. [29]
В качестве металлоиндикатора на ионы К ( 1) применяют нитхромазо, который обеспечивает хорошую индикацию конечной точки титрования при Я, 626 нм. Этим методом определяют 0 8 - 50 000 Mkr СЮз и 0 7 - 1400 мке СЮ. Присутствие 100-кратных количеств ионов С1 -, Вг -, F -, SQl -, NOJ, а также ЭДТА не влияет на точность определения. [30]
Страницы: 1 2 3
