Присутствие - молекула
Cтраница 2
Для расчета не принято во внимание присутствие молекул D2O, что не вносит большой ошибки, так как а для Н20 - HDO и HDO - D2O одинаковы, а константа равновесия реакции H20 D2O2HDO близка к четырем. [16]
 |
Зависимость общего. [17] |
Закон Рауля выполняется тогда, когда присутствие молекул В не влияет на взаимодействие между молекулами А. Давление пара РА при этом зависит от сил взаимодействия между молекулами А и от их количества в растворе. [18]
Эта реакция, повидимому, требует присутствия молекулы воды в момент столкновения. [19]
Для протекания этого процесса обычно необходимо присутствие я-связанных молекул, например СО, R3P и других, конкурирующих за место в координационной сфере металла и способствующих восстановительному сочетанию. Примеры таких процессов-приведены в разд. [20]
Величина М № очень чувствительна к присутствию молекул более высокого молекулярного веса, а величина Мп - от молекл более низкого молекулярного веса. [21]
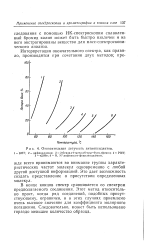 |
Относительная летучесть антиоксидантов. [22] |
Это дает возможность создать представление о присутствии определенных молекул. [23]
Эти данные позволяют нам предположить, что присутствие молекул воды на активном центре алюмосиликата ( алюминия с координационным числом 4) понижает его активность в реакции полимеризации изобутилена. Активность алюмосиликата возрастает по мере удаления воды с поверхности минерала. При полном удалении воды катализатор обладает максимальной активностью. Прокаливание силлиманита при температурах выше 700 С приводит, вероятно, уже к его спеканию. [24]
К межмолекулярным следует отнести и водородные связи; присутствие ие-полярных молекул или углеводородных цепей увеличивает среднюю упорядоченность воды, обусловленную этими связями; поэтому удаление неполярных компонентов из воды приводит к частичному разупорядочиванию, повышая энтропию системы; этот процесс рассматривается как гидрофобное взаимодействие между неполярными группами. [25]
Неравноценность связей Мо-О в Na2MoO4 2Н2О явно вызвана присутствием молекул воды: два атома О, находящиеся на наибольших расстояниях от Мо, образуют с молекулами воды водородные связи. [26]
Жидкий раствор данного вещества отличается от газообразной фазы присутствием молекул растворителя. Поскольку последние не принимают участия в кристаллизации растворенного вещества, влияние их сводится к затруднению перехода его из раствора в кристаллическую фазу. [27]
Жидкий раствор кристаллизуемого вещества отличается от газообразной фазы присутствием молекул растворителя. Поскольку последние не принимают участия в кристаллизации растворенного вещества, влияние их сводится к затруднению перехода его из раствора в кристаллическую фазу. Это влияние может быть учтено путем умножения скорости кристаллизации, рассчитанной для газа ( с той же самой концентрацией молекул), на вероятность того, что молекула растворенного вещества находится в газоподобном состоянии. [28]
Однако наше рассмотрение взаимодействия С12 со стенкой в присутствии молекул Н2 может быть не достаточно полно. Выше мы уже указывали, что, повидимому, следует признать возможным процесс Н2 С12 НС1 Н С1 - 58 ккал. Однако вследствие большой эндотермичности в объеме этот процесс не может играть сколько-нибудь существенной роли. [29]
Однако наше рассмотрение взаимодействия С12 со стенкой в присутствии молекул Н2 может быть не достаточно полно. Выше мы уже указывали, что, по-видимому, следует признать возможным процесс Н2 С12 НС14 - Н С1 - 58 ккал. Однако вследствие большой эндотермичности в объеме этот процесс но может играть сколько-нибудь существенной роли. [30]
Страницы: 1 2 3 4