Присутствие - едкий натр
Cтраница 2
Натриевая соль глюконовой кислоты в присутствии едкого натра играет роль ловушки кальция и поэтому используется в составе щелочных средств для мытья бутылок. Она также способна связывать ионы железа в широком диапазоне рН и как препятствующий отложению железа агент применяется в составе щелочных препаратов для борьбы со ржавчиной. Кальциевые и железные соли глюконовой кислоты применяются как пероральные и внутривенные препараты в медицине, а чистая кислота - как моющее средство в молочной промышленности. Глюконолактон находит применение как медленно действующий подкислитель в составе пекарских порошков, при переработке мяса и в других отраслях пищевой промышленности. [16]
Водорастворимые смолы, полученные в присутствии едкого натра или едкого кали, содержат небольшое количество диме-тиленэфирных связей - СН2 - О - СН2 -, из которых при нагревании выделяется формальдегид. [17]
В PC, полученной в присутствии едкого натра или едкого кали, имеется некоторое количество простых эфирных связей - СН2 - - О - СН2 - и при нагревании ее выделяется формальдегид. [18]
Ацетон при действии о-нитробензальдегида в присутствии едкого натра образует индиго. К 10 мл исследуемого водного раствора содержащего не более 20 мг ацетона, прибавляют 15 капель свежеприготовленного 1 % - ного раствора о-нитробензальдегида в 50 % - ном спирте и 0 5 мл 30 % - ного раствора едкого натра. Через некоторое время появляется окраска - от желтовато-зеленой до зеленовато-синей. При большем количестве ацетона выпадает синий осадок индиго, который можно извлечь хлороформом. [19]
Процесс селективной очистки метанолом в присутствии едкого натра позволяет удалить до 99 % меркаптанов, содержащихся в бензине. [20]
Сультам был получен пиролизом триазена в присутствии едкого натра и порошка меди. [21]
Конденсация бензальдегида с ацетоном происходит в присутствии едкого натра. [22]
Сультам был получен пиролизом триазена в присутствии едкого натра и порошка меди. [23]
Исульфо ислоты в сильнощелочной среде в присутствии едкого натра, сначала при температуре 100 - й02, а затем при температуре 90 в течение нескольких часов. [24]
При взаимодействии с раствором йода в присутствии едкого натра образуется йодоформ; при кипячении с раствором едкого натра в присутствии резорцина возникает розовое окрашивание Чистоту препарата определяют по нейтральной реакции спиртового раствора и отсутствж) хлоридов. [25]
Так как растворимость сульфата натрия в присутствии едкого натра с повышением концентрации NaOH снижается, основное количество Na2SO4 ( около 40 - 50 кг на I т 92 % - ного NaOH) кристаллизуется вместе с небольшим количеством NaCl из концентрированных растворов едкого натра на последней стадии выпарки. [26]
В промышленности эту реакцию проводят в присутствии едкого натра. В реактор загружают раствор едкого натра, анилин и затем сероуглерод. Реактор герметически закрывают и нагревают реакционную массу при размешивании до 35 - 40 С. При этом в аппарате возникает небольшое избыточное давление. После спуска избыточного давления к реакционной массе постепенно добавляют раствор бисульфита натрия, который разлагает побочный продукт реакции ( натриевую соль тритио-угольной кислоты) с выделением сероуглерода. Выделяющийся сероуглерод связывается со второй половиной загруженного анилина. [27]
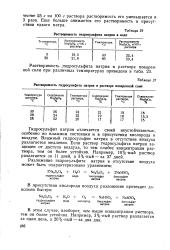 |
Растворимость гидросульфита натрия в воде.| Растворимость гидросульфита натрия в растворе поваренной соли. [28] |
Еще больше снижается его растворимость в присутствии едкого натра. [29]
Закрепляются они на волокне плюсованием в присутствии едкого натра с последующим запариванием. [30]
Страницы: 1 2 3 4