Присутствие - озон
Cтраница 1
Присутствие озона в атмосфере также обязано действию ультрафиолетовых лучей. Кислород переходит в озон даже при действии излучений радия, полония, эманации и других радиоактивных элементов. [1]
Присутствие озона в атмосферном воздухе является показателем чистоты последнего, так как озон играет большую роль в защите воздуха от бактерий. Содержание озона более 0 005 мл в 1 мл воздуха вызывает головокружение, головную боль и плохое самочувствие. Таким образом, биологический порог действия озона начинается при содержании его более 0 005 мл в 1 л воздуха. [2]
Присутствие озона в воздухе создает серьезные негативные проблемы, ибо он ( активнейший окислитель, используемый человеком для дезинфекции) разрушает некоторые молекулы, играющие большую роль в биологических процессах, ослабляет иммунную систему человека и поражает легочную ткань. В совокупности с кислотными осадками и углеводородами озон считается виновником замедления роста и гибели лесов в Европе. [3]
В присутствии озона обе бумажки синеют; лакмусовая - от наличия КОН, а крахмальная - от присутствия молекулярного иода. [4]
В присутствии озона раствор окрашивается в фиолетовый цвет. На приборе можно измерять также концентрации хлора, сероводорода и других токсичных веществ, для которых известны колориметрические реакции. [5]
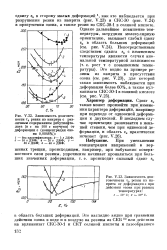
В присутствии озона при Н Н0 наблюдается растрескивание с постоянной скоростью dcldN v, которая не зависит от Н, а определяется только концентрацией озона. Зависимость dcldN от Н выше Н0 объясняется Лейком и Линдлеем механохимическими и чисто механическими процессами. [6]
 |
Простейший озонатор. [7] |
Этим объясняется присутствие озона в воздухе хвойных лесов. [8]
Этан в присутствии озона окисляется до уксусного альдегида и уксусной кислоты. [9]
Ненасыщенные углеводороды очень чувствительны к присутствию озона даже в очень малых концентрациях, в которых он имеется в атмосфере. Атмосферная концентрация изменяется от нуля до нескольких частей на 10 частей воздуха. [10]
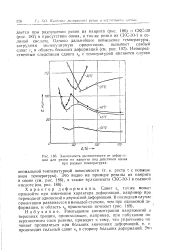 |
Зависимость долговечности от деформации для резин из наирита под действием озона при разных температурах. [11] |
СКС-30 ( рис. 187 в присутствии озона, а также резин из СКС-30-1 в со-ляной кислоте. [12]
Показано, что скорость окисления в присутствии озона гораздо выше, чем без него, полная энергия активации при этом равна 8 - 9 ккал моль. В полимере в ходе окисления накапливаются группировки ОН, СО и С-О - С. При окислении азотной кислотой при низких температурах происходит главным образом разрыв С - С-связей полимерных молекул; при высоких температурах имеет место нитрование. Полная энергия активации равна 35 6 ккал / моль. Инфракрасные спектры поглощения продуктов разложения полиэтилена при 400 и 440, полученные Хельвеге, Кайзером и Лампе [638] путем конденсирования в высоком вакууме на пластинку NaCl, отличаются от спектров обычного полиэтилена появлением полосы олефиновых групп при 11 мк. [13]
СКС-30 ( рис. V.24) в присутствии озона, а также резин из GKC-30-1 в соляной кислоте. [15]
Страницы: 1 2 3 4