Присутствие - незначительная примесь
Cтраница 1
Присутствие незначительных примесей влияет на свойства катализатора. [1]
Присутствие незначительных примесей меди также вызывает покраснение катодных осадков. Наличие солей серебра вызывает побеление осадков. Медь и серебро иногда специально вводят в электролит для получения цветного золочения. [2]
Наряду со структурой via сорбционные свойства большое влияние оказывает влажность и присутствие незначительных примесей кислот, оставшихся на силикагеле после его обработки. [3]
Диалкилпероксиды ( низкомолекулярные члены ряда) - жидкости или твердые вещества с невысокими температурами плавления ( ниже 100 С), хотя некоторые из них плавятся выше 150 С, обычно с сильным разложением. Температуры плавления зависят от скорости нагревания и от присутствия незначительных примесей ( катализаторов разложения), поэтому некоторые опубликованные значения могут невоспроизводиться. [4]
Нами было исследовано влияние примесей раствора соли трехвалентного железа Fe на кинетику взаимодействия брома с 1 2-дибромпропаном. Можно сделать чисто качественный вывод о том, что присутствие незначительных примесей Fe ( 10 - 5 м) резко замедляет течение реакции бромирования. Причина этого явления нами подробно не изучалась. По-видимому, одна из возможных причин этого явления заключается в следующем: соли трехвалентного железа в растворах гидролизуются, и подкисление, вызванное этим, смещает равновесие ( 1) в сторону образования начальных продуктов. [5]
Митчел и Смит [1], в экспериментах Китинга и Скотта наблюдалось обратное явление: более устойчивым оказался реактив, приготовленный на техническом продукте. Все эти факты свидетельствуют о том, что скорость уменьшения водной функции реактива Фишера, по-видимому, зависит от присутствия незначительных примесей посторонних веществ, возможно, неорганического происхождения. Выяснение природы этих ингибиторов разложения реактива Фишера является чрезвычайно важной задачей практической акваметрии. [6]
 |
Фракционирование изотопов в процессе окисления. [7] |
Процедура получения пробы SO2 заключается в следующем. Для анализа берут навеску сульфида, содержащую примерно 8 мг серы; это обеспечивает достаточное количество газа SO2, при котором не сказывается присутствие незначительных примесей посторонних газов при масс-спектрометрическом определении изотопного состава серы. [8]
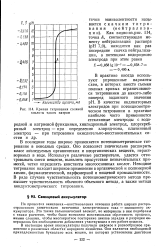 |
Кривая титрования соляной. кислоты едким натром. [9] |
В последние годы широко применяется потенциометрическое титрование в неводных средах. Оно позволяет значительно расширить класс исследуемых органических и неорганических веществ, нерастворимых в воде. Используя различные растворители, удается отти-тровывать смеси веществ, выявлять присутствие незначительных примесей, четко определять константы многоосновных кислот. Неводное титрование находит широкое применение в органической и полимерной химии, фармацевтической, парфюмерной и пищевой промышленности. В ряде случаев чувствительность потенциометрического метода превышает чувствительность обычного объемного метода, а также метода кондуктометрическогс титрования. [10]
Для выяснения фазового состава обесфторенного фосфата, полученного в полузаводских опытах, применялись кристал-лооптический и рентгенографический методы анализа. Установлено также присутствие незначительной примеси тетра-кальцийфосфата. Показатели преломления близки к показателям для а-трикальцийфосфата, однако угол оптических осей меньше, чем для трикальцийфосфата. Установлено присутствие небольшого количества второй фазы с более высокими показателями светопреломления ( Ug 1 640 и Np 1 634), ближе всего соответствующими тетракальцийфосфату. Прорастания этих двух фаз отчетливо видны в шлифах. В иммерсионных препаратах присутствуют незначительные количества мелких кристалликов гексагональной формы с JVml64, что соответствует фторапатиту. [11]
Изучение органических соединений с известным строением показало, что сумма атомных парахоров с большой точностью совпадает с молекулярным парахором данного вещества. Сравнение молекулярных объемов по методу парахор оказалось наилучшим из всех предложенных методов, так как величина парахора не зависит от температуры. Следует упомянуть, что в более поздних работах можно найти указание на некоторое расхождение между парахорами и суммами атомных и групповых парахоров для металлоорганических соединений а также соединений с галоидами, серой, мышьяком и фосфором. Парахор смесей практически подчиняется правилу слагаемое, причем присутствие незначительных примесей сернистых или кислородных соединений не нарушает этих свойств. [12]
Парахор обладает большим сходством с молярной рефракцией. Каждый атом в молекуле имеет определенную величину парахора, называемую инкрементом, причем такими же инкрементами обладают двойные и тройные связи и различные кольца. Молярный парахор получается сложением инкрементов всех атомов, связей и колец, имеющихся в молекуле. Парахор смесей обладает свойствами аддитивности. Как показали работы Мардера [232], в присутствии незначительных примесей кислородных и сернистых соединений свойства аддитивности углеводородных смесей моторных топлив не нарушаются. [13]
Измерения обычно проводятся на малых образцах в калориметре с теплообменным газом, так как большие кристаллы алмаза почти недоступны. Подробные измерения были проведены де Сорбо, образец которого содержал почти 7 моль мелких алмазов с размером зерен - 2 мм. Вследствие трудностей, отмеченных выше, экспериментальная погрешность при температурах ниже 70 К была довольно велика, чем, возможно, и объясняется максимум в около 60 К. Появление максимума кажется весьма странным, поскольку измерения на веществах с кристаллической решеткой типа алмаза, проведенные до температур, при которых уже заведомо выполняется закон Ts, не дают никаких указаний на наличие такого максимума. Результаты де Сорбо систематически лежат ниже результатов Питцера, полученных несколько ранее, однако это расхождение можно объяснить присутствием незначительных примесей в каждом образце. [14]
Измерения обычно проводятся на малых образцах в калориметре с теплообменпым газом, так как большие кристаллы алмаза почти недоступны. Подробные измерения были проведены де Сорбо, образен, которого содержа. Вследствие трудностей, отмоченных выше, экспериментальная погрешность при температурах ниже 70 К была довольно велика, чем, возможно, и объясняется максимум У около ( 0 К. Появление максимума кажется весьма странным, поскольку измерения на веществах с кристаллической решеткой типа алмаза, проведенные до температур, при которых уже заведомо выполняется закон Т Л, не дают никаких указаний на наличие такого максимума. Результаты де Сорбо систематически лежат ниже результатов Питцера, полученных несколько ранее, однако ото расхождение можно объяснить присутствием незначительных примесей в каждом образце. [15]
Страницы: 1