Присутствие - след - металл
Cтраница 1
Присутствие следов металлов в эфирных маслах способствует прогорканию жиров в пищевых и косметических изделиях, огду-шенных ими, появлению пятен на кусках мыла и порче парфюмерных композиций. [1]
Гидролиз сахарозы, катализируемый ферментом р-фруктофу-ранозидаза ( инвертаза), замедляется в присутствии следов металлов, являющихся ингибиторами. Микроколичества анионов, образующих устойчивые комплексы с этими металлами, например ионов цианидов, сульфидов и иодидов, понижают ингибиторное действие металлов. [2]
Обширные опыты Сирла, Ла-Кэ и Дароу6 показали, что цвет вина в большей степени зависит от присутствия следов металла, чем вкус и букет вина; 3 ш / л и даже меньшие количества железа или олова уже оказывают влияние на оттенок вина; цинк и никель действуют слабее. [3]
Вследствие большой восстановительной силы аскорбиновой кислоты растворы ее быстро окисляются, причем окисление это значительно ускоряется в присутствии следов металлов, проявляющих каталитическое действие. [4]
Таким образом весовой формой является Сг2О3, а ртуть npi прокаливании улетучивается. В присутствии следов щелочныз металлов осадок окисляется частично в хромат. Ввиду этого если предполагается присутствие ионов щелочных металлов осадок нужно тщательно промывать. [5]
Но растворы аскорбиновой кислоты неустойчивы. Скорость разложения их зависит, прежде всего, от чистоты препарата. Окисление значительно ускоряется в присутствии следов металлов, проявляющих каталитическое действие. Раствор аскорбиновой кислоты может разлагаться также под воздействием бактерий. [6]
Но растворы аскорбиновой кислоты неустойчивы. Скорость разложения их зависит, прежде всего, от чистоты препарата. Окисление значительно ускоряется в присутствии следов металлов, проявляю - ж, щих каталитическое действие. Раствор аскорбиновой кислоты может разлагаться также под воздействием бактерий. [7]
Но растворы аскорбиновой кислоты неустойчивы. Скорость разложения их зависит, прежде всего, от чистоты препарата. Окисление значительно ускоряется в присутствии следов металлов, проявляющих каталитическое действие. Раствор аскорбиновой кислоты может разлагаться также под воздействием бактерий. [8]
Кислород вызывает быстрое превращение тиолов в дисульфиды. Эта реакция количественно протекает и под действием других окислителей. Так, йод используется для объемного определения меркаптанов. Эта реакция каталитически ускоряется присутствием следов металлов, в частности меди и железа. Реакция протекает быстрее при рН выше 7 в присутствии гидрата окиси аммония или щелочных металлов в качестве катализаторов. Скорость реакции, по-видимому, возрастает с повышением концентрации применяемой щелочи. [9]
Основное применение аскорбиновой кислоты - прямое титрование ею Fe3 [9, 17], кроме того, ее используют для определения хлоратов, иодатов, броматов, VO. Но растворы аскорбиновой кислсты неустойчивы. Скорость разложения их зависит, прежде всего, от чистоты препарата. Окисление значительно ускоряется в присутствии следов металлов, проявляющих каталитическое действие. Раствор аскорбиновой кислоты может разлагаться также под воздействием бактерий. [10]
Как правило, легкость аутоокисления углеводородов снижается в последовательности алкилароматические диолефиновые мо-ноолефиновые парафиновые. Аутоокисление парафинов при низких температурах не протекает; поэтому выделить промежуточные продукты аутоокисления не удается. Аутоокисление олефинов протекает при температурах 25 - 125 С С в зависимости от структуры исходного соединения. Обычно при таких низких температурах удается выделить гидроперекиси. Присутствие следов металлов заметно снижает энергию активации реакции аутоокисления - иногда на 20 ккал / моль. Щелочи также ускоряют окисление, но длина реакционных цепей окисления при этом уменьшается, так как промежуточные формы связываются основанием. [11]
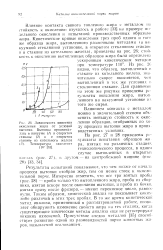 |
Зависимость кинетики лению образцов, отобранных по ходу процесса вытопки жира в производственных условиях. [12] |
Результаты испытаний показывают, что чем позже от начала процесса вытопки отобран жир, тем он менее стоек к окислительной порче. Интересно отметить, что все три взятых пробы ( рис. 28) - проба только что вытопленного жира, проба из сборника, взятая вскоре после окончания вытопки, и проба из бочки, взятая сразу после фрпзера - имеют перекисное число, равное нулю. Таким образом, химический анализ не показывает каких-либо различий в этих трех пробах. В то же время кинетический метод анализа, примененный в рассматриваемой работе, позволяет обнаружить изменение свойств жира на тех стадиях, когда существующие химические методы анализа еще не регистрируют никаких изменений. Присутствие следов металлов [ 35J способствует развитию одной из разновидностей порчи животных жиров, называемой осаливанием. [13]
Соотношение количества соли и раствора составляло 1: 1 ( по весу) стой целью, чтобы различие в свойствах солей были более отчетливы. Концентрация растворов определялась потенциометрически, как описано в [19], после промывки растворов горячей дистиллированной водой и осушки поташом в течение суток. Достоверность результатов была проверена сравнением данных, полученных по методу Кьельдаля и потенциомет-рического титрования. Было установлено, что присутствие следов металлов в титруемом растворе не влияет на положение точки эквивалентности. Таким образом была определена степень удаления азота из бензольных растворов пиридина и хинолина солями железа - хлорным, хлористым, азотнокислым окисным, ферри-цианидсм калия и хлористым цинком. [14]
Остается дать сведения о чистоте поверхностей окислов, с которыми мы работали. Хотя судить об этом очень трудно, мы считаем, что наши препараты, по существу, не содержали газообразных загрязнений, однако никакие меры против паров смазки и ртути не принимались. В описанной выше работе окислы обезгаживали при температурах между 510 и 640 в течение 18 час. При таком методе поглощенные газы должны были удаляться и все же проводились опыты с целью проверить и определить количество любых загрязнений. При работе с ZnO были получены относительно большие количества Н2, образовавшегося, по-видимому, в результате присутствия следов металла в междуузлиях ( окись цинка готовили сжиганием Zn на воздухе); не считая этого, ни в одном случае содержание других имевшихся газов не превышало количества, необходимого для покрытия 5 % поверхности окисла. [15]
Страницы: 1 2