Присутствие - углекислота
Cтраница 4
Хорошо известно, что соли радия, как, например, бромид, хлорид и в меньшей степени карбонат, постепенно окрашиваются под действием собственного излучения. В случае бромида и хлорида одновременно наблюдается увеличивающееся разложение солей под действием излучения, которое в присутствии углекислоты воздуха большей частью ведет к образованию карбоната в случае сульфата радия. [46]
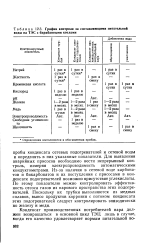 |
График контроля за составляющими питательной воды на ТЭС с барабанными котлами. [47] |
Для выявления аварийных присосов необходимо вести непрерывный контроль, измеряя электропроводимость автоматическими кондуктометрами. Из-за наличия в сетевой воде карбонатов и бикарбонатов и их поступления с присосами в конденсате подогревателей возможно присутствие углекислоты. [48]
В очень мягкой воде дождевая вода и некоторые минеральные 1воды) коррозия труб продолжается неопределенно долго. К счастью, большинство вод, употребляемых для водоснабжения, содержат значительное количество углекислого кальция, который в присутствии углекислоты находится в растворе в виде двууглекислого кальция. Если избыток углекислоты имеется в количестве, достаточном только для удержания углекислого кальция в растворе, то начинающаяся коррозия вызовет возрастание значения рН у катодных участков и, следовательно, приведет к осаждению углекислого кальция; это перенесет катодную реакцию в Другое место, так что спустя некоторое время вся внутренняя поверхность трубы покроется слоем углекислого кальция, который в присутствии достаточного количества кислорода будет взаимодействовать с солями железа, находящимися под ним, с образованием пристающей окисно-железной ржавчины. Получившийся смешанный слой, который часто обладает значительным защитным характером, может быть описан как меловая ржавчина, или ржавый мел. Во многих водах этот слой более защитен, если кислород присутствует в больших количествах, потому что ржавчина в этом случае образуется в тесном контакте с металлом. Взаимодействие между углекислым кальцием и закисными солями железа, вероятно, вначале дает закисное углекислое железо, которое затем окисляется. В отсутствии избытка кислорода магнетит часто отстает от металла и является не очень защитным веществом. [49]
Другая проблема заключается в получении чистого цианида из сырой смеси после азотирования. Вода не является подходящим растворителем, так как цианистый натрий в растворе частично гидролизован, в особенности в присутствии углекислоты воздуха. Кроме того не прореагировавший карбонат, так же как и цианид, растворим в воде, что увеличивает затруднения при получении цианида высокой степени чистоты. [50]
Страницы: 1 2 3 4