Присутствие - восстановитель
Cтраница 2
В присутствии восстановителя оксид железа или соответственно обожженная железная руда хлорируется с образованием FeCls. В случае смеси хлора и оксида углерода реакция протекает энергично при 460 С, в присутствии фосгена - при 350 С. [16]
В присутствии восстановителей ( С, S, Ы2, СО, СН4) темп - pa термич. [17]
В присутствии восстановителей определение кислорода целесообразно проводить по Россу: в кислородную склянку приливают сначала 0 5 мл H2SO4 ( I: 4), а затем 0 5 мл смешанного раствора NaCIO и Na2SO4; после этого ее закрывают пробкой, взбалтывают и ставят в темное место на 30 мин. Для устранения избытка NaCIO добавляют 1 мл раствора KCNS и взбалтывают. Через 10 мин приступают к определению кислорода. [18]
В присутствии восстановителя SnCl2 окраска переходит в коричневую, а чувствительность реакции снижается. Метод пригоден для определения 2 - 50 мкг Re в 10 мл раствора. Окраска достигает максимальной интенсивности при нагревании растворов до 80 С в течение 10 - 15 мин. Окрашенное соединение экстрагируется хлороформом. Окраска экстракта устойчива, если раствор защищен от воздуха и солнечных лучей. Определению рения не мешают хлориды и перхлораты. Сульфаты снижают интенсивность окраски ( если их более 1 г на 15 мл); нитраты мешают определению и их необходимо удалять. Перекись водорода действует аналогично. [19]
В присутствии восстановителей, в том числе и НС1, происходит восстановление окислителей и MnOi; поэтому нельзя подкислять растворы соляной кислотой. [20]
В присутствии восстановителей малиново-красная окраска пермангаката обесцвечивается. Нагревание на водяной бане способствует протеканию реакции окисления - восстановления. [21]
В присутствии восстановителей ( например, S - ионов) бурая окраска иода обесцвечивается. [22]
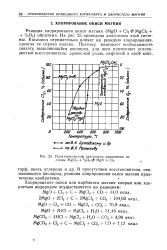 |
Политермическая диаграмма равновесия системы MgCl2 / 2О2 MgO С12. [23] |
В присутствии восстановителя, связывающего кислород, реакция хлорирования окиси магния практически необратима. [24]
В присутствии восстановителей, в том числе и НС1, происходит восстановление окислителей и МпО; поэтому нельзя подкислять растворы хлористоводородной кислотой. [25]
В присутствии восстановителей малиново-красная окраска перманганата обесцвечивается. Нагревание на водяной бане способствует протеканию реакции окисления - восстановления. [26]
В присутствии восстановителей ( например, 52 - - ионов) бурая окраска иода обесцвечивается. [27]
В присутствии восстановителей, катионы IV и V аналитических групп ведут себя как окислители и восстанавливаются до соединений низших степеней окисления или до свободных металлов. Пря действии сильных окислителей Си -, РЬ2 - и В13 - ионы окисляются до высшей степени окисления. [28]
В присутствии восстановителя, например Ыа25Оз, иод, выделяющийся по второй реакции, снова переходит в иодид и таким образом обеспечивается полный перевод его в нерастворимое соединение CuJ, которое легко отфильтровывается. [29]
В присутствии восстановителей катионы IV и V аналитических групп ведут1 себя как окислители и восстанавливаются до соединений низших степеней окисления или до свободных металлов. При действии сильных окислителей ионы Си, РЬ2 и Bi3 окисляются до высшей степени окисления. [30]
Страницы: 1 2 3 4