Большее притяжение
Cтраница 1
 |
Действие гравитационного поля на гантелевидную систему. из-за небольшого различия в силе притяжения каждой частицы, находящейся на различном расстоянии от гравитирующего центра, создается момент. [1] |
Большее притяжение испытывает ближайшая к гравитирующему центру частица, слабее притягивается более удаленная частица. При любой другой ориентации момент стремится развернуть стержень в верти-кальное положение. [2]
Большее притяжение высокого положительного заряда центрального иона к отрицательному заряду лигандов проявляется в уменьшении способности лигандов координационного комплекса связываться с другими катионами. В ряду VO4 -, СгО4 - и МпО4 - ванадат-ион представляет собой очень сильное основание и способен связываться с протоном Н или другими катионами. Хромат-ион также является довольно сильным основанием. [3]
Главной причиной отрицательных отклонений реальных смесей от идеальных является наличие больших притяжений между разнородными молекулами ХА и ХБ, чем между однородными молекулами ХА и ХА, а также ХБ и ХБ, то есть наличие тенденции к химическому соединению двух веществ. [4]
Молекула 2 испытывает меньшее притяжение вверх со стороны молекул пара и большее притяжение вниз со стороны молекул жидкости. [5]
 |
К понятию о поверхностном натяжении. [6] |
Молекулы жидкости, находящиеся на поверхности ее раздела с газом, испытывают значительно большее притяжение со стороны жидкости, чем со стороны газовой среды, отличающейся малой плотностью. Вследствие этого возникает направленная внутрь жидкости сила, стремящаяся переместить ее молекулы с поверхности в глубину. Поверхность жидкости ведет себя подобно туго натянутой резиновой пленке. [7]
Ориентируясь своим положительным полюсом по направлению к катоду, коллоидная частица испытывает к нему большее притяжение, чем к далеко расположенному аноду, и поэтому двигается к катоду. [8]
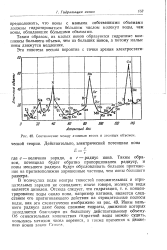 |
Соотношение между атомным весом и атомным объемом. ческой теории. Действительно, электрический потенциал иона. [9] |
Таким образом, потенциал будет обратно пропорционален радиусу, и ионы меньшего радиуса будут обусловливать большее притяжение на противоположно заряженные частицы, чем ионы большего размера. [10]
Отсюда следует, что когда точка возвращается из М в Ж, она следует в сторону большего притяжения и сумма работ сил притяжения к двум противоположным граням будет положительна. [11]
Наличие большего электрического заряда, чем у магния и, особенно натрия, вызывает с гидроокиси алюминия значительно большее притяжение кислородного и отталкивайте водородного атома и обусловливает ее слабо осн овные свойства. [12]
Из этого определения кислоты и основания вытекает, что все атомы, характеризующиеся большой электроотрицательностью, должны образовывать кислотные соединения, так как, обладая большим притяжением к отрицательным зарядам-электронам, слабо притягивают положительные заряды-протоны; атомы, характеризующиеся малой электроотрицательностью, наоборот, должны образовывать основания. Отсюда же следует, что в высших валентных состояниях все элементы проявляют кислотные свойства, так как электроотрицательность атома возрастает по отношению к последовательному ряду его валентных электронов. Следовательно, элементы обладают кислотным или основным характером, и это, естественно, объясняется таким основным свойством атома, как электроотрицательность. [13]
Из этого определения кислоты и основания вытекает, что все атомы, характеризующиеся большой электроотрицательностью, должны образовывать кислотные соединения, так как, обладая большим притяжением к отрицательным зарядам-электронам. Отсюда же следует, что в высших валентных состояниях все элементы проявляют кислотные свойства, так как электроотрицательность атома возрастает по отношению к последовательному ряду его валентных электронов. Следовательно, элементы обладают кислотным или основным характером, и это, естественно, объясняется таким основным свойством атома, как электроотрицательность. [14]
Из этого определения кислоты и основания вытекает, что все атомы, характеризующиеся большой электроотрицательностью, должны образовывать кислотные соединения, так как, обладая большим притяжением к отрицательным зарядам-электронам, слабо притягивают положительные заряды-протоны; атомы, характеризующиеся малой электроотрицательностью, наоборот, должны образовывать основания. Отсюда же следует, что в высших валентных состояниях все элементы проявляют кислотные свойства, так как электроотрицательность атома возрастает по отношению к последовательному ряду его валентных электронов. Следовательно, элементы обладают кислотным или основным характером, и это, естественно, объясняется таким основным свойством атома, как электроотрицательность. [15]
Страницы: 1 2 3