Заполнение - поверхность - электрод
Cтраница 2
 |
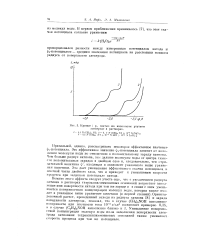
Зависимость тока восстановления а-бромкапроновой кислоты при постоянном потенциале ( на подъеме волны от ее приэлектродной концентрации. [16] |
При достаточно высоких ск, когда заполнение поверхности электрода деполяризатором приближается к полному, нижняя часть полярограмм перестает зависеть от ск [11], а так как их верхняя часть становится с ростом с выше и смещается к более отрицательным потенциалам, то и значение Jf. Этим же, вероятно, объясняется и некоторое несовпадение величин ДЯ. [17]
 |
Кривые t ф, снятые на капельном ртутном электроде в растворах. [18] |
Уменьшение поверхностной концентрации молекул веды из-за заполнения поверхности электрода катионами тстраалкиламмониевых оснований также уменьшает скорость процесса при том же потенциале. [19]
При одинаковом количестве осаждаемого металла степень заполнения поверхности электрода кристаллами, очевидно, определяется размерами кристаллов. Если кристаллы крупные, то лишь небольшая часть поверхности электрода будет покрыта осадком, в то время как при таком же количестве осаждаемого металла с мелкими кристаллами, вся поверхность будет равномерно покрыта осадком. [20]
 |
Схема капиллярного алектрометра Гун. [21] |
Заряд электрода является функцией потенциала электрода и степени заполнения поверхности электрода молекулами адсорбата. [22]
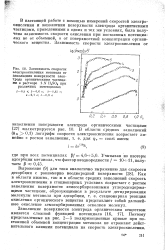 |
Зависимость скорости электроокисления метанола от заполнения поверхности электрода органическими частицами в растворе 1N H2S04 при различных потенциалах. [23] |
В настоящей работе с помощью измерений скоростей электроокисления и заполнения поверхности электрода органическими частицами, проведенными в одних и тех же условиях, была получена зависимость скорости окисления при постоянных потенциалах не от объемной, а от поверхностной Концентрации органического вещества. [24]
Однако они могут быть использованы для исследования изменений степени заполнения поверхности электрода. [25]
Влияние органических ингибиторов на скорость электродных процессов определяется степенью заполнения поверхности электрода молекулами ингибитора. Особый интерес представляет установление зависимости между адсорбируемостью органических веществ, степенью торможения электродного процесса и особенностями строения их молекул. [26]
Увеличение энергии связи водорода с металлом приводит к возрастанию заполнения поверхности электрода адсорбированными атомами водорода и, следовательно, к повышению скорости рекомбинации. Однако одновременно увеличивается энергия активации стадии рекомбинации, так как более прочно связанным с поверхностью атомам труднее вступить во взаимодействие друг с другом, чем связанным слабо. Поэтому, как и в стадии разряда, зависимость тока обмена рекомбинационной стадии от энергии связи водорода с металлом должна проходить через максимум. [27]
В - константа адсорбционного равновесия; в - степень заполнения поверхности электрода; а - аттракционная постоянная. [28]
Увеличение энергии связи водорода с металлом приводит к возрастанию заполнения поверхности электрода адсорбированными атомами водорода и, следовательно, к повышению скорости рекомбинации. Однако одновременно увеличивается энергия активации стадии рекомбинации, так как более прочно связанным с поверхностью атомам труднее вступить во взаимодействие друг с другом, чем связанным слабо. Поэтому, как и в стадии разряда, зависимость тока обмена рекомбинационной стадии от энергии связи водорода с металлом должна проходить через максимум. [29]
Из уравнения ( 11) легко найти, как должно изменяться заполнение поверхности электрода при с const вследствие протекания процесса электроокисления хемосорбированных частиц. [30]
Страницы: 1 2 3 4