Взаимное притяжение - атом
Cтраница 1
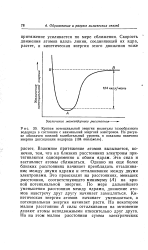
Взаимное притяжение атомов вызывается, конечно, тем, что на близких расстояниях электроны притягиваются одновременно к обоим ядрам. Эта сила и заставляет атомы сближаться. Однако на еще более близких расстояниях начинает преобладать отталкивание между двумя ядрами и отталкивание между двумя электронами. Это происходит на расстояниях, меньших расстояния, соответствующего минимуму ( А) на кривой потенциальной энергии. По мере дальнейшего уменьшения расстояния между ядрами, движение атомов навстречу друг другу начинает замедляться. Кинетическая энергия атомов начинает уменьшаться, а потенциальная энергия начинает расти. На некотором малом расстоянии Б силы отталкивания на мгновение делают атомы неподвижными относительно друг друга. [2]
Вследствие взаимного притяжения атомов и молекул соприкасающихся или сблизившихся на очень малые расстояния тел появляются силы взаимодействия этих тел. При измерениях притяжения тел Б. В. Дерягин установил, что сила такого взаимодействия обратно пропорциональна расстоянию между поверхностями тел в шестой степени. [3]
 |
Колебание молекулы. [4] |
Валентная связь означает взаимное притяжение атомов, обусловленное перекрыванием электронных облаков. Но атомы притягиваются не безгранично: они ведь не сливаются друг с другом. Атомные ядра валентно связанных атомов устанавливаются на определенном расстоянии друг от друга - на равновесном расстоянии. При дальнейшем сближении атомов в игру вступают силы отталкивания: нельзя втиснуть одно электронное облако в другое больше определенной степени перекрывания. Следовательно, равновесное расстояние между атомами есть то расстояние, на котором силы притяжения уравновешены силами отталкивания. [5]
Увеличение U12 с расстоянием соответствует взаимному притяжению атомов. Точка минимума С / 12 соответствует некоторому устойчивому равновесию. [6]
С увеличением межатомных расстояний значительно возрастают силы взаимного притяжения атомов. При снятии напряжений под действием сил притяжения атомы возвращаются в исходное положение и упругая деформация исчезнет. [7]
С увеличением межатомных расстояний значительно возрастают силы взаимного притяжения атомов. При снятии напряжения под действием этих сил атомы возвращаются в исходное положение, искажение решетки ( ее упругая деформация) исчезает. [8]
Следует, однако, подчеркнуть, что идея о взаимном притяжении атомов серы имеет далеко идущие последствия. S в призмах равны 3 15 - 3 18 А. Тот факт, что призматическая координация осуществляется у одних и тех же металлов с одинаковыми неметаллами и и в особенности сохранение почти тех же расстояний 4 Mo-S как в MoS2, так и в Мо ( 82С2Н2) 35свидетельствует, по-видимому, об однотипности характера связи в бесконечной системе MoS2 и в замкнутой системе комплекса. С другой стороны, аналогичное резкое сокращение межлиганцных расстояний в семивершинном комплексе Mo ( NO) fS2CNBu2 ] 3, где также наблюдается почти полное равенство расстояний S... S внутри и между циклами ( среднее значения 2 81 и 3 02 А), позволяет перенести идею о межлигандном сопряжении и на другие координации металла, где число вершин, их взаимное расположение и размеры атомов лиганда требуют расстояний на 0 6 - 0 7 А меньше суммы их невалентных радиусов. Таким образом, характеристика химических связей в бинарных структурах переходных металлов становится все более сложной. [9]
В хороших растворителях исключенный объем возрастает, напротив, в плохих растворителях взаимное притяжение атомов цепи больше, чем их притяжение к молекулам растворителя, и объемные эффекты уменьшаются. Очевидно, что речь идет о явлении, аналогичном наблюдаемому в точке Бойля реального газа. При температуре Бойля отталкивание молекул компенсируется их взаимным притяжением. [10]
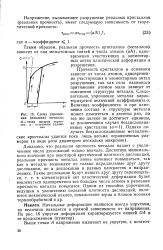 |
Схема упрочнения ( наклепа металла. [11] |
Прочность кристаллов в основном зависит от числа атомов, Одновременно участвующих в элементарных актах разрушения, так как сила взаимного притяжения атомов мало зависит от изменения структуры металла. [12]
Для того чтобы смещение атомов в новые положения равновесия не приводило к нарушению сплошности, необходимо, чтобы в процессе такого смещения атомы не удалялись один от другого на расстояния большие, чем размеры зоны активного действия сил взаимного притяжения атомов. [13]
Молекулы углеводородов расщепляются при нагреве их до высоких температур. Силы взаимного притяжения атомов в молекуле противодействуют разрыву. Однако при достаточно высокой температуре связи между атомами в молекулах ослабевают настолько, что под влиянием колебательного движения атомов происходит разрыв связи. [14]
Приведенное выражение показывает, что сорбционные взаимодействия проявляются только на очень малых расстояниях. Теоретически, если взаимное притяжение атомов максимально на расстоянии г0, то при г 1 5 г0 их взаимодействие ослабевает в 4 - 5 раз. И наоборот, при г 0 5 г0 превалируют силы отталкивания [ 32, с. Иногда дисперсионные взаимодействия усиливаются водородными связями и электростатическими ( индукционными или ориентационными) силами. Эти дополнительные взаимодействия специфичны для определенного вида сорбируемых веществ или свойств поверхности сорбента. Сорбция - процесс самопроизвольный, протекающий с выделением некоторого количества теплоты. [15]
Страницы: 1 2