Причина - изменение - активность
Cтраница 1
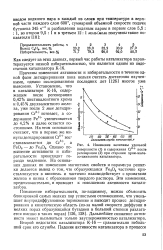 |
Изменение величины удельной поверхности ( 1 и содержания Сг6 после регенерации ( 2 при старении хром-железо-цинкового катализатора. [1] |
Причины изменения активности и избирательности в течение одной фазы дегидрирования пока нельзя считать достаточно изученными, однако исследованиями последних лет [126] многое уже выяснено. Установлено, что в катализаторе К-16, содержащем после регенерации 0 42 % шестивалентного хрома и 0 45 % двухвалентного железа, уже после 2 мин дегидрирования Сг6 исчезает, а содержание Fe2 увеличивается до 4 2 % и далее остается постоянным. Однако повышение активности и избирательности происходит гораздо медленнее. На основании данных по изменению магнитных свойств и параметра решетки делается вывод о том, что образующаяся Fe3O4 частично кристаллизуется в шпинель и частично взаимодействует с хроматами железа и цинка с образованием твердого раствора. Эти изменения, предположительно, и приводят к повышению активности катализатора. [2]
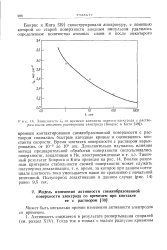 |
Зависимость i0 от времени контакта медного электрода с раствором после анодного растворения электрода ( Бокрис и Кита. [3] |
Может быть несколько причин изменения активности электродов со временем. [4]
Астрофизики продолжают искать всюду в Галактике данные, которые позволили бы лучше понять причины изменения активности в прошлом, настоящем ив будущем. [5]
Хотя характер изменения активности катализатора в цикле относительно каждой из реакций установлен, причины изменения активности еще не совсем ясны. [6]
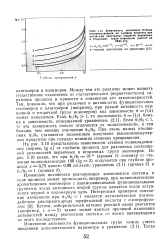 |
Зависимость логарифма степени поликонденсации от глубины процесса при различных константах скорости первичвых н вторичных групп мономеров ( расчет на ЭВМ 17. [7] |
Изменение активности реагирующих компонентов системы в ходе процесса может происходить, например, при поликонденсации ароматических мономеров с взаимозависимыми функциональными группами, когда активность второй группы меняется после вступления первой в полимерную цепь. Кстати, избирательный катализ реакций одних реагентов ( например, с п 2) также может явиться причиной изменения активностей между реагентами системы со всеми вытекающими из этого последствиями. [8]
В частности, в работе, проведенной с полиморфными разновидностями кобальта, выявлены весьма малые изменения дисперсности; было совершенно очевидным, что различия активности вызваны только фазовым превращением. Если же взять большой интервал температур, когда возможна сильная рекристаллизация, тогда оказывается трудным определить соотношения между этими двумя причинами изменения активности. [9]
В реакциях жидкофазного окисления углеводородов ведущую роль играют перекисные радикалы RO. J, а скорость окисления определяется их активностью и концентрацией. За последнее время в работах [1-4], посвященных изучению реакций окисления, сформулированы некоторые причины изменения активности свободных радикалов под влиянием растворителей. Перекисные радикалы могут образовывать водородные связи с гидроксилсодержащими молекулами растворителя [4], вследствие чего их активность снижается. Ароматические углеводороды ( бензол и его производные) образуют с перекисными радикалами - комплексы [1,5], что снижает их активность. При окислении полярных соединений необходимо учитывать влияние диэлектрической постоянной на реакцию RO. С другой стороны, присутствие полярного растворителя увеличивает скорость распада гидроперекисей ( главных поставщиков свободных радикалов в реакциях жидкофазного окисления углеводородов) за счет неспецифической сольватации молекул гидроперекиси растворителем. В отдельных случаях существенную роль играет специфическая сольватация - ассоциация посредством водородных связей гидроперекиси между собой при их больших концентрациях или с электроноакцепторными соединениями ( например: гидроперекись третичного бутила-пиридин [6], гидроперекись изопропилбензола-нитробен-зол [7], что приводит к увеличению скорости распада, а следовательно, и к концентрации свободных радикалов. [10]
Баландина и Борка [257], Баландина и Либермана [259] были получены первые точные уравнения кинетики каталитических реакций в проточной системе, открывшие широкие возможности количественного экспериментального изучения парофазно-го гетерогенного катализа и процессов отравления катализаторов дегидрогенизации. Изучение дегидрогенизации и дегидратации спиртов на окиси магния, предпринятое Рубинштейном и Прибытковой [261] в связи с цитированной работой Баландина и Рубинштейна [256], привело также к важным выводам: установлена причина изменения активности катализатора в зависимости от способа его приготовления. Рубинштейн и Прибыткова установили существование оптимального параметра решетки для катализа при одинаковой дисперсности катализатора. Впоследствии Рубинштейн совместно с Куликовым [262], Прибытковой [263, 264], Куликовым и Захаровым [265] также преимущественно на реакциях дегидрогенизации - дегидратации спиртов установили некоторые причины избирательности катализаторов по отношению к указанным реакциям. Эти причины связаны с изменением структуры катализаторов: с изменением фазового состава, с деформацией решетки, с появлением включений. [11]
Поскольку изменения в величинах энергий активации, по-видимому, не являются причиной различия в активностях исследованных катализаторов, то это различие должно быть обусловлено разными значениями частотных факторов. На основе предположения о постоянстве энергии активации были рассчитаны частотные факторы для каждого образца катализатора. Одной из причин изменения активности являются различия в удельной поверхности металла; поэтому в найденные на опыте значения были внесены соответствующие поправки, учитывающие влияние удельной поверхности. [12]
Хиноны легко взаимодействуют с аминокислотами. Так, еще в 1927 г. Опарин показал способность системы хлорогеновая кислота - фенолоксидаза дезаминировать аминокислоты. Способность хи-нона реагировать с сульфгидрильными амино - и иминогруппами является причиной связывания хинонов с белками. Именно эта способность хинонов может явиться причиной изменения активности ферментов. Так, Вильяме ( Williams, 1960), а затем Салькова и Платонова ( 1968) показали, что в процессе ферментативного окисления фенолов наибольшее снижение активности полигалактуро-назы вызывали первичные продукты окисления фенолов. [13]
Эта формула применима для всех концентраций катализатора и независит от характера и концентрации присутствующей соли. Указывалось, что эта формула применима не только для омыления сложных эфиров, но также для инвер - сии Сахаров и других близких реакций. Акерлеф полагал, что это является доказательством неправильности теории каталитической активности недиссоциированных молекул. Он утверждал, что молекула соли не имеет собственной активности, а является лишь причиной изменений активности катализаторов. Акерлеф также ответил на вопрос, касающийся способа, которым нейтральные соли изменяют активность катализатора, утверждая, что сольватные слои из молекул воды вокруг водородного иона меняются в результате добавления нейтральных солей. Таким образом, концентрация водородных ионов сохраняется постоянной, но их активность изменяется. Согласно этой точки зрения гидрат-ные числа - неопределенные числа; они характеризуют изменения силы, с которой различные ионы притягивают молекулы воды, изменения этой силы обусловлены действием различных нейтральных солей. Путем сравнения гид-ратных чисел, полученных в результате исследований, Реми [413] и Уошборн с сотрудниками [498, 499, 500] пришли к заключению, что самое сильное действие нейтральной соли наблюдается для ионов, которые гидратируются в большой степени. Этой гипотезе противоречит равенство действия нейтральных солей для всех нитратов, между тем как для хлоридов действие меняется от одной соли к другой. [14]
Страницы: 1