Проба - перекись - водород
Cтраница 1
Пробы перекиси водорода отбирают стеклянным или алюминиевым тщательно промытым пробоотборником в чистые ополоснутые перекисью водорода склянки. Горловины склянок закрывают стеклянными пробками с капиллярными отверстиями для выхода газа и завязывают полихлорвиниловой пленкой. [1]
Пробы перекиси водорода отбирают стеклянным или алюминиевым тщательно промытым пробоотборником в чистые ополоснутые перекисью водорода склянки. Среднюю пробу тщательно перемешивают и помещают в две склянки. Горловины склянок закрывают стеклянными пробками с капиллярными отверстиями для выхода газа или завязывают полихлорвиниловой пленкой. [2]
При вводе в пробу перекиси водорода включают секундомер и пробу перемешивают. С интервалом времени в 1 мин растворы гидрохинона и перекиси водорода вводят во все стаканы. Через 20 мин раствор из первого стакана переливают в кювету ( / 00 мм) и измеряют оптическую плотность растворов на фотоэлектроколори-метре ФЭК-М с зеленым светофильтром. С интервалом в 1 - 2 мин проводят измерение оптической плотности растворов остальных проб. По данным измерений оптической плотности растворов первых шести проб строят калибровочный график в координатах оптическая плотность D - концентрация меди. По графику определяют концентрацию меди в анализируемых пробах воды. [3]
Механические примеси определяют фильтрованием пробы перекиси водорода и последующим взвешиванием оставшегося на фильтре осадка. [4]
Нелетучий остаток определяют путем выпаривания пробы перекиси водорода в платиновой чашке с последующим взвешиванием остатка. Платина чашки катализирует разложение перекиси водорода. Прокаливанием и взвешиванием нелетучего остатка определяют прокаленный остаток. [5]
Нелетучий остаток определяют путем выпаривания пробы перекиси водорода в платиновой чашке с последующим взвешиванием остатка. Платина чашки катализирует разложение перекиси водорода. [6]
Механические примеси определяют посредством фильтрования пробы перекиси водорода и последующего взвешивания оставшегося на фильтре осадка. [7]
Нелетучий остаток определяют путем выпаривания пробы перекиси водорода в платиновой чашке с последующим взвешиванием остатка. Платина чашки катализирует разложение перекиси водорода. [8]
Механические примеси определяют посредством фильтрования пробы перекиси водорода и последующего взвешивания оставшегося на фильтре осадка. [9]
Результаты вполне сравнимы с получаемыми методами титрования. Очевидные преимущества этого метода с применением иммерсионного рефрактометра - удобство и быстрота-снижаются в связи с затратами па приобретение прибора, а также необходимостью иметь довольно значительную пробу. Если же пользоваться более удобным рефрактометром Аббе, для которого нужна небольшая проба, приходится сталкиваться с проблемами тщательного контроля температуры и защиты пробы перекиси водорода от каталитического разложения. Если необходимо поставить большое число серийных анализов, то рефрактометрический метод часто оказывается наиболее быстрым и удобным. Рефрактометр должен быть снабжен специальными призмами ( поставляемыми той же фирмой), позволяющими снизить размер разложения до минимума. [10]
В табл. 59 представлены массы и распространенность изотопов водорода и кислорода. Поскольку и водород и кислород являются относительно легкими атомами, изменение изотопного состава молекулы перекиси водорода сравнительно сильно изменяет ее молекулярный вес. Однако в связи с тем, что тяжелые изотопы присутствуют в природе лишь в очень малых относительных количествах, необходимо во много раз обогатить пробу естественной перекиси водорода тяжелыми изотопами, чтобы средний молекулярный вес смеси заметно повысился. Возможность такого обогащения в процессе производства ( например, при электролизе или перегонке), по-видимому, ничтожно мала. [11]
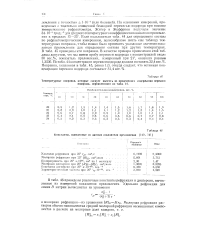 |
Константы, выведенные из данных показателя преломления. [12] |
На основании измерений, проведенных с тщательно очищенной безводной перекисью водорода при помощи иммерсионного рефрактометра, Жигер и Жоффрион получили значение 34 - 10 а град. Если пользоваться табл. 44 для определения состава по рефрактометрическим измерениям, целесообразно иметь еще таблицу температурных поправок, чтобы можно было применить указанные значения показателя преломления для определения состава при других температурах. В табл. 45 приведены эти поправки. В качестве примера применения этой таблицы допустим, что мы имеем пробу перекиси водорода с концентрацией около 30 вес. По табл. 44 концентрация перекиси водорода должна составить 32 4 вес. Поправка, указанная в табл. 45, равна 1 0, откуда следует, что истинная концентрация перекиси водорода составляет 31 4 вес. [13]
Примерно к тому времени, когда началось производство перекиси водорода, возник интерес к вопросам ее стабильности и возможности работы с концентрированными растворами. Типичным для последней явились результаты работы Харкурта [59], который утверждал, что стекло, нарочно загрязненное маслом или лакированное, предотвращает разложение разбавленной перекиси водорода значительно лучше, чем чистое стекло. Шепе [60] в 1878 г. указал, что противоречивые высказывания относительно свойств перекиси водорода, возможно, обусловливаются присутствием в пей примесей. Проба перекиси водорода, способная к выделению 9 объемов кислорода из одного объема раствора, стоявшая в лаборатории Дэвиса, за 11 недель разложилась на 20 %; после добавления нескольких капель эфира дальнейшего разложения не наблюдалось в течение 8 недель. Вертело [61], изучавший скорости разложения в течение месяца и более, пришел к выводу, что стабильность зависит от отсутствия щелочи в растворе. [14]
Страницы: 1